HISAKOの美容通信2027年4月号
皮膚のお話|免疫・代謝・バリアの恒常性から、個々の病態と老化を理解する事は、最適な治療の選択に繋がる
 皮膚は、私達の体を外界から保護する重要なバリア機能を担うだけでなく、免疫、感覚、代謝等の多彩な機能を備えた最大の臓器です。皮膚は、単なる外壁ではなく、免疫系や代謝ネットワークの中心として、生体内外の相互作用を調節する非常にダイナミックなシステムとして機能しています。更には、皮膚は外界とダイレクトに接しており、肉眼での観察が可能で、組織サンプルの採取も容易で、又多光子励起顕微鏡等の先端技術を導入し易い等々の臓器特性から、発生・構造から疾患のメカニズムの解明、更には新規治療法の開発に至るまで、近年目覚ましい進歩を遂げている臓器でもあります。
皮膚は、私達の体を外界から保護する重要なバリア機能を担うだけでなく、免疫、感覚、代謝等の多彩な機能を備えた最大の臓器です。皮膚は、単なる外壁ではなく、免疫系や代謝ネットワークの中心として、生体内外の相互作用を調節する非常にダイナミックなシステムとして機能しています。更には、皮膚は外界とダイレクトに接しており、肉眼での観察が可能で、組織サンプルの採取も容易で、又多光子励起顕微鏡等の先端技術を導入し易い等々の臓器特性から、発生・構造から疾患のメカニズムの解明、更には新規治療法の開発に至るまで、近年目覚ましい進歩を遂げている臓器でもあります。
TOKIO KUMAGAIって、デザイナーを覚えていますか? 1980年代にフランス・パリのモード業界で、モノトーンのシックな紐靴というシンプルなデザインのみならず、身近な動物や鳥や花、昆虫に、食べ物、有名なアート作品をモチーフにした、アバンギャルド且つユーモアと独創性溢れる独創性な靴を多数デザイン発表し、足元のファッションの彩りを増やした、新進気鋭のファッションデザイナーでした。活動期間が10年にも満たずに、40歳の若さでAIDSで亡くなりました(←当時、付き合っていたと噂のあった三宅一生に感染されたと言う、実しやかな噂話が流布されていましたが…84歳までと、三宅一生がほぼ天寿を全うした事を思うと、単なるフェイクニュースだったのでしょうねぇ)。旭川のド田舎の医大生だったHISAKOは、雑誌でたまたま見掛けた彼の象革製の靴が欲しくて欲しくて…、地図を片手に(Google マップなんてない時代でしたから!)、彼のブティックを探して代官山を彷徨したのを覚えています。…当時、皮膚科と言うものに対して全く興味がなかった医学生のHISAKOの、最初に興味を激しくそそったのが、人間ではなくて象の皮膚だった。ただそれだけのお話なんですけどね(笑)。あの頃は若く、皺もシミも皆無でしたから、所謂布(皮膚科)よりも、その立体的な造形(形成外科)に惹かれていました。
今まで、美容通信では、皮膚の治療に関する断片的な皮膚のお話しか書いてなかったな、と今更ながら思い、今回の特集となりました。
皮膚概論
皮膚の恒常性の維持と破綻
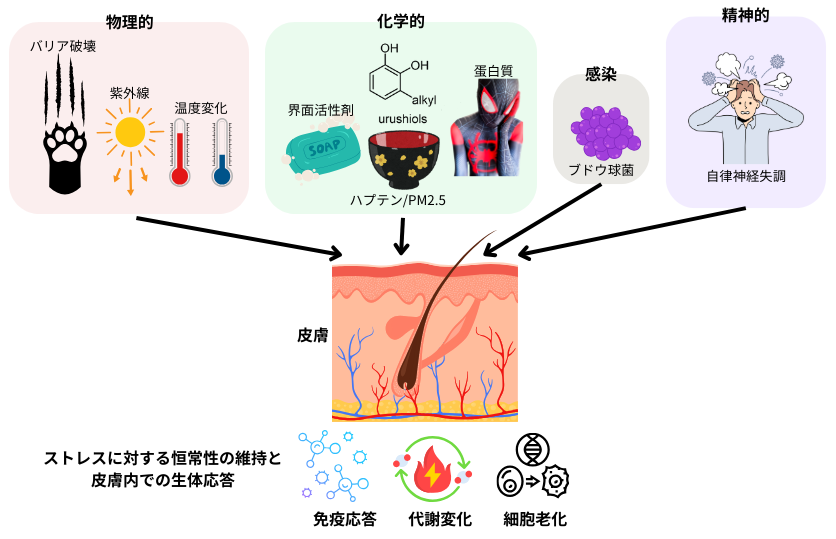
 皮膚は、外界と直接接触する最大の臓器であり、紫外線、温度変化、乾燥、大気汚染、微生物感染等の多彩な環境ストレスに常時暴露されています。これ等のストレスに対し、皮膚は適応的な生体応答を誘導し、恒常性を維持する高度な制御機構を有しています。皮膚内部では、免疫系の活性化、代謝変化、細胞老化と言った多岐に亘る生理的プロセスが恒常的に進行しており、これ等の相互作用が皮膚の恒常維持に不可欠です。
皮膚は、外界と直接接触する最大の臓器であり、紫外線、温度変化、乾燥、大気汚染、微生物感染等の多彩な環境ストレスに常時暴露されています。これ等のストレスに対し、皮膚は適応的な生体応答を誘導し、恒常性を維持する高度な制御機構を有しています。皮膚内部では、免疫系の活性化、代謝変化、細胞老化と言った多岐に亘る生理的プロセスが恒常的に進行しており、これ等の相互作用が皮膚の恒常維持に不可欠です。
■表皮:バリア機能の基盤とフィラグリン
角層は皮膚の最も外側の層で、主な構成細胞である表皮角化細胞(ケラチノサイト)がミルフィーユの様に10層ほど積み重なっており、0.2mm程度の厚さを構成しています。血管がないので、専ら、真皮から基底膜を介して栄養を分けてもらう代わりと言っては何ですが、水分保持や異物侵入防止の役割を担う物理的なバリアとして機能します。この機能は、フィラグリンやケラチンを含む蛋白質と、セラミドや脂肪酸等の細胞間脂質によって支えられています。髪結いの亭主とかヒモとか雄ライオンとか…様々な比喩はありますが、彼らは単なる木偶の坊では務まりません。これ等の構成要素を適切に形成する事で、初めて、皮膚は、外界からの刺激や病原体から生体を保護する事が可能になります。水分の蒸発だって防げます。
フィラグリン遺伝子の変異(美容通信2014年11月号)は、アトピー性皮膚炎の発症リスクを高めるだけでなく、食物アレルギーや喘息と言った他臓器のアレルギー疾患にも深く関与します。これは、皮膚バリアの破綻により、異物が経皮的に感作される経皮感作のプロセスが、全身の免疫系に影響を及ぼす事を示唆しています。最近の研究では、アトピー性皮膚炎リスクのある乳幼児に対する、早期スキンケアや外用ステロイドによる治療介入が、皮膚のみならず、他臓器のアレルギー疾患の予防に寄与する可能性が示されています。この様な介入は、アレルギー疾患の発症予防戦略として、今後の医療に於いて重要な位置を占めると考えられています。
■マイクロバイオームと皮膚免疫の相互作用
皮膚表面には約1兆個の微生物が生息し、これ等のマイクロバイオームは、病原体の侵入を防ぐバリアとして機能するだけでなく、皮膚免疫応答を適切に調節する為の情報伝達を担っています。
健常な皮膚では、表皮ブドウ球菌、コリネバクテリウム属等の善玉菌が、黄色ブドウ球菌の増殖を抑制し、皮膚バリアを守る役割を果たしています。しかし、アトピー性皮膚炎では、黄色ブドウ球菌の増殖に伴い、毒素や炎症因子を分泌する事で、皮膚のバリアが損傷され、皮膚炎が増悪します。近年、マイクロバイオームを標的とする治療法(美容通信2024年2月号)が注目されています。マイクロバイオームをリバランスする外用剤の臨床試験も進行中であり、これ等の治療法は、アトピー性皮膚炎やニキビ、乾癬等の疾患に於いて、大きな可能性を秘めています。
■環境因子と皮膚恒常性
紫外線、乾燥、大気汚染と言った環境因子は、皮膚のバリア機能や恒常性に深刻な影響を与え、皮膚疾患の発症や悪化に関与するだけでなく、恐ろしい事に、皮膚を老化させます。特に紫外線は、ビタミンD合成(美容通信2013年3月号)の様な功の面だけではなく、DNA損傷や活性酸素種(ROS)(美容通信2017年10月号)の生成を介して、皮膚細胞に直接的なダメージを与える負の側面もあります。これにより、皮膚のバリア機能は損なわれ、炎症や乾燥が誘発されてしまいます。また、紫外線の暴露は、色素沈着やコラーゲンの分解を促し、所謂光老化を加速させます。環境因子により、表皮細胞の再生能力の低下やコラーゲン・エラスチンの分解、血管機能の低下等が引き起こされ、結果、皮膚の老化が進んでしまいます。
■生体防御反応としての痛み・痒み
痛みや痒みは、皮膚の病気で良く認められる症状で、一種の生体防御反応です。
 アトピー性皮膚炎の痒みには、Th2細胞が産生するIL-31が重要な役割を果たしています。IL-31は、末梢神経のIL-31受容体に作用し、痒み信号を活性化しますが、2023年に発売された生物製剤ミチーガ(ネモリズマブ)は、末梢神経のIL-31受容体を標的とするお注射です。
アトピー性皮膚炎の痒みには、Th2細胞が産生するIL-31が重要な役割を果たしています。IL-31は、末梢神経のIL-31受容体に作用し、痒み信号を活性化しますが、2023年に発売された生物製剤ミチーガ(ネモリズマブ)は、末梢神経のIL-31受容体を標的とするお注射です。
皮膚の免疫について
皮膚の重要な生理的機能の一つは、外的異物の侵入防御です。この機能を発揮する為に、皮膚は角質層やタイトジャンクション等の物理的なバリアと、種々の免疫応答を介した免疫学的なバリアの2つのバリアを兼ね備えています。後者の免疫学的バリアとは、皮膚に侵入した多種多様な微生物・抗原等の外的異物に対し、皮膚に存在する様々な免疫細胞達が迅速に応答し、お互いに助け合いながら、それらの異物の排除を行っています。しかしながら、その一方で、過剰な免疫応答は自分自身を却って傷つけてしまう事になるので、過剰な免疫応答が生じない様に、生体は免疫応答を負に制御するメカニズムを複数有しています。その制御メカニズムのバランスが何らかの原因により崩れてしまうと、接触皮膚炎を代表とする種々のアレルギー反応やアトピー性皮膚炎、乾癬等の疾患の発症に繋がってしまいます。
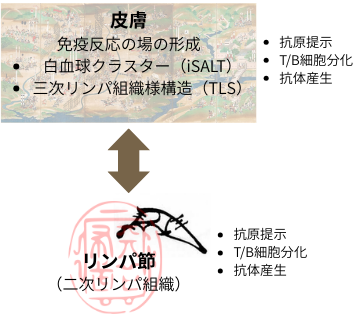 皮膚には、表皮角化細胞、線維芽細胞、血管内皮細胞、リンパ管内皮細胞等の上皮・間葉系細胞群と、樹状細胞、マクロファージ、肥満細胞、リンパ球(T細胞)、自然リンパ球等の血球系細胞群があり、更には、神経系細胞や、毛包、脂腺、汗腺、爪等の付属器の構成細胞等も混在しています。これ等の皮膚に存在するあらゆる細胞は、夫々独自に、又、種々の細胞と相互作用を行い、直接的、間接的に皮膚の免疫反応に関与しています。しかし、この様な効率的な応答を可能にしているのが、tertiary lymphoid structure(三次リンパ構造)やinducible skin associated lymphoid tissue(誘導型皮膚関連リンパ様組織)等の、皮膚に形成される独特の場の存在です。野戦築城とか、戦闘陣地と表現した方が、イメージが付きやすいかも知れません。皮膚の炎症や癌、自己免疫疾患等の病態の進展や制御に関与していると考えられています。
皮膚には、表皮角化細胞、線維芽細胞、血管内皮細胞、リンパ管内皮細胞等の上皮・間葉系細胞群と、樹状細胞、マクロファージ、肥満細胞、リンパ球(T細胞)、自然リンパ球等の血球系細胞群があり、更には、神経系細胞や、毛包、脂腺、汗腺、爪等の付属器の構成細胞等も混在しています。これ等の皮膚に存在するあらゆる細胞は、夫々独自に、又、種々の細胞と相互作用を行い、直接的、間接的に皮膚の免疫反応に関与しています。しかし、この様な効率的な応答を可能にしているのが、tertiary lymphoid structure(三次リンパ構造)やinducible skin associated lymphoid tissue(誘導型皮膚関連リンパ様組織)等の、皮膚に形成される独特の場の存在です。野戦築城とか、戦闘陣地と表現した方が、イメージが付きやすいかも知れません。皮膚の炎症や癌、自己免疫疾患等の病態の進展や制御に関与していると考えられています。
宣教師伝いでイタリア戦争について知っていたとされる織田信長の長篠の戦いが、日本に於ける野戦築城の萌芽とされていますが、野戦築城の目的は、城や要塞と比較して拠るべきものが少ない野外という環境に於いて、効果的な陣地を作り防御をしつつ、敵軍を誘引撃滅する事です。永久要塞と異なり、野戦軍は移動する事が常であり、野戦築城には一時的な或いは簡易な要塞としての性質が求められます。左図は、旧日本軍のトーチカの写真ですが、硫黄島の戦いでは、旧日本軍陣地は極めて大規模であり、洞穴(地下)陣地とトーチカを巧みに組み合わせた永久要塞に匹敵するものでした。
■皮膚に於ける免疫反応の場:tertiary lymphoid structure(三次リンパ構造;TLS)
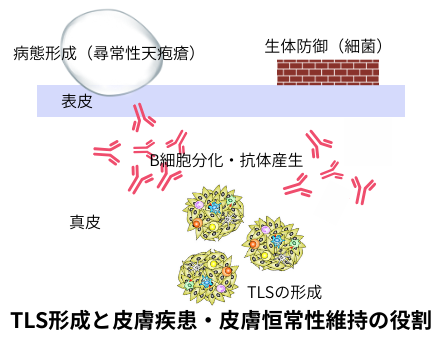 末梢組織に形成される、リンパ節や脾臓に似た構造体。リンパ節の様に被膜には包まれてはいないものの、T細胞やB細胞等の免疫細胞によって構成されていて、リンパ節の様に濾胞構造を有しています。リンパ節に於ける特殊な血管である高内皮細静脈 (high endothelial venules : HEV) の、マーカー(PNAd)を発現する血管も出現します。炎症や癌、自己免疫疾患等の際に様々な臓器でTLSは形成され、皮膚に於いても、TLS類似構造が幾つかの皮膚疾患で認められています。例えば、皮膚の自己免疫疾患である尋常性天疱瘡では、皮膚でTLSが形成され、自己抗体産生・治療抵抗性に寄与していると考えられています。
末梢組織に形成される、リンパ節や脾臓に似た構造体。リンパ節の様に被膜には包まれてはいないものの、T細胞やB細胞等の免疫細胞によって構成されていて、リンパ節の様に濾胞構造を有しています。リンパ節に於ける特殊な血管である高内皮細静脈 (high endothelial venules : HEV) の、マーカー(PNAd)を発現する血管も出現します。炎症や癌、自己免疫疾患等の際に様々な臓器でTLSは形成され、皮膚に於いても、TLS類似構造が幾つかの皮膚疾患で認められています。例えば、皮膚の自己免疫疾患である尋常性天疱瘡では、皮膚でTLSが形成され、自己抗体産生・治療抵抗性に寄与していると考えられています。
未だ人間でも同様の減少が生じるかどうかまでは分かっていませんが、マウスでの研究では、表皮ブドウ球菌の皮膚へのcolonizationは、リンパ節に於ける抗体産生(IgG1、IgG3)誘導のみならず、皮膚に於けるTLS形成を誘導し、制御性T細胞が濾胞T細胞に分化し、TLS内でIgG2b、IgG2c産生誘導を行い、細菌からの防御機構に重要な役割を果たしています。
■アレルギー性接触皮膚炎に於ける免疫応答の場の形成:inducible skin associated lymphoid tissue(誘導型皮膚関連リンパ様組織;iSALT)
接触性皮膚炎みならず、アトピー性皮膚炎や尋常性乾癬では、皮膚内に抗原特異的T細胞を効率的に活性化する為の新たな免疫応答の場として、リンパ様組織構築(Skin-Associated Lymphoid Tissue; SALT)が、一過性に誘導されます。
皮膚細菌叢
 皮膚常在菌叢(美容通信2024年2月号)は、宿主の皮膚免疫系のバランスを不可欠な役割を担っており、皮膚細菌叢の乱れが様々な皮膚疾患の発症や増悪の原因となる事が、近年明らかになって来ています。特に、アトピー性皮膚炎に於いては、Syaphylococcus aureusを中心とした細菌による疾患の発症・増悪の機序解明が進んでいます。S. aureusのAgrクオラムセンシングシステムは、アトピー性皮膚炎の発症・増悪に重要な役割を果たすと考えられており、これをターゲットとした治療戦略も試みられるようになって来ました。
皮膚常在菌叢(美容通信2024年2月号)は、宿主の皮膚免疫系のバランスを不可欠な役割を担っており、皮膚細菌叢の乱れが様々な皮膚疾患の発症や増悪の原因となる事が、近年明らかになって来ています。特に、アトピー性皮膚炎に於いては、Syaphylococcus aureusを中心とした細菌による疾患の発症・増悪の機序解明が進んでいます。S. aureusのAgrクオラムセンシングシステムは、アトピー性皮膚炎の発症・増悪に重要な役割を果たすと考えられており、これをターゲットとした治療戦略も試みられるようになって来ました。
皮膚常在菌叢と皮膚免疫
大人の皮膚は、毛包やエクリン汗腺、アポクリン汗腺、皮脂腺内の上皮を含めると、表面積として凡そ30m2に達するとされ、そこには多様な常在微生物が存在し、1cm2当たり106個の細菌がいます。新生児の皮膚細菌叢は、主に分娩時に獲得される為、帝王切開で生まれたか、経膣分娩だったかによって変わります。前者では、お母さんの皮膚細菌叢に近く、後者では、膣微生物叢に近くなります。この様な差異は、後々の皮膚細菌叢及び免疫系の発達に長期的な影響を及ぼすと考えられています。長じるに従って、皮膚細菌叢は徐々に変動し、思春期には、特に皮脂腺が発達する領域で大きな変化が起こりますが、大人になると、比較的安定した状態に落ち着きます。私達人間の皮膚は、新生児期から成人期にかけて、メモリー制御性T細胞を段階的に獲得し、常在菌に対する免疫寛容を手にします。
マウス新生仔に於いて、皮膚常在菌の代表種であるStaphylococcus epidermidisがコロニーを形成すると、CD4+制御性T細胞が皮膚に移動し、常在菌に対する免疫寛容が生じます。また、S. epidermidisは、病原性微生物に対する防御機能を担うIL-17A+CD8+T細胞の誘導を促進し、Candida albicansやLeishmania major等の病原菌に対する自然免疫を強化します。Staphylococcus属のうち、S. epidermidis、S. hominisは、私達人間の皮膚に常在する代表的なコアグラーゼ陰性ブドウ球菌ですが、S. aureus等の病原細菌を標的とした抗菌ペプチドを産生します。加えて、常在菌のStaphylococcusは、宿主を刺激して、病原性微生物の排除を助けるβ-ディフェンシン-2等の抗菌ペプチドを産生させます。また、従来、ニキビの原因となる悪玉菌の代表格として考えられていたCutibacterium acnesが放出する代謝産物は、皮膚バリア機能や免疫反応を強化する可能性が報告されています。つまり、皮膚細菌叢全体としての総合的な機能が見直されつつあります。
皮膚常在菌叢と皮膚疾患
■アトピー性皮膚炎
アトピー性皮膚炎(美容通信2024年2月号)(美容通信2007年4月号)(美容通信2014年11月号)は、表皮バリア異常やアトピー素因等の遺伝子背景に加え、衛生仮説に代表される環境因子の相互作用で発症すると考えられています。この様な環境要因の一つが、皮膚細菌叢のdysbiosis(バランス異常)と考える事も出来ます。
*衛生仮説:幼少期に、微生物や寄生虫等に十分な曝露してないと、免疫系の発達が適切に進まないので、免疫応答をアレルギー優位に傾け、その結果、アレルギー疾患のリスクが高まるとする考え方。まあ、多少はばばっちい方が、元気に子供は育つ!って説ですね。
- アトピー性皮膚炎に於けるdyabiosisの特徴
アトピー性皮膚炎の病変部では、菌叢の多様性の低下やStaphylococcus属の増加を特徴とするdyabiosisが起こっていて、健常人では定着し得ないS. aureusがコロニーを形成していたり、S. epidermidisの異常繁殖が屡々認められます。報告によれば、アトピー性皮膚炎の患者さんのS. aureusの保有率は約70%ですが、重症度が酷くなればなる程、増加する事が知られています。更には、S. aureusは変異を起こしながら、人間の皮膚に適応して、家族内で世代を超えて引き継がれる事も知られており、これがアトピー性皮膚炎の遺伝性に一役買っている可能性も指摘されています。
常在細菌叢に存在するS. epidermidisは、普通は、セリンプロテアーゼであるEspの産生により、S. aureusによるバイオフィルムの形成を阻害し、定着を防ぎ、常在細菌叢の安定を図る善玉菌です。ところが、アトピー性皮膚炎の患者さんの病変皮膚では、EcpAを産生するS. epidermidisの菌株が増加し、皮膚炎を酷くする事も知られており、増殖する菌株によって善にも悪にもなります。
アトピー性皮膚炎では、細菌以外の微生物の関与も知られています。皮膚常在真菌で最も一般的に認められるMalassezia属ですが、アトピー性皮膚炎ではコロニー形成が認められ、重症度と比例して増加する事も分かっています。Malasseziaの蛋白質抗原が、炎症性サイトカインの産生を亢進させ、結果、皮疹を増悪させます。
- S. aureusがアトピー性皮膚炎を増悪させるメカニズム
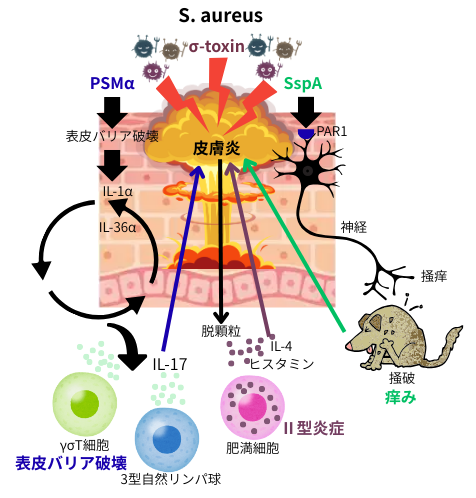 S. aureusは、様々な病原因子によってアトピー性皮膚炎を増悪させます。その中でも特に重要視されているのが、accessory gene regulator(agr)と称される遺伝子群によって制御されるクオラムセンシングシステムです。S. aureusは、このシステムにより、自身の菌の生息密度を感知し、毒素の産生をコントロールしています。S. aureusのAgr-QSの下流で発現する毒素のσ-toxinは、マスト細胞の脱顆粒を引き起こして、Th2炎症を誘発ます。PSMαは、表皮バリア破壊を引き起こし、ケラチノサイトからのアラーミンであるIL-1α及びIL-36α等のサイトカインの放出を誘導して、IL-17依存性の皮膚炎を惹起して、アトピー性皮膚炎の皮膚症状を悪化させます。また、Agr-QSの下流のSspAは、神経系のPAR1受容体を介して、痒みを誘発させます。つまり、S. aureusは、Agr-QSの活性化により、アトピー性皮膚炎の重要な3病態とされる、Th2免疫と表皮バリア破壊、痒みの全てを悪化させます。
S. aureusは、様々な病原因子によってアトピー性皮膚炎を増悪させます。その中でも特に重要視されているのが、accessory gene regulator(agr)と称される遺伝子群によって制御されるクオラムセンシングシステムです。S. aureusは、このシステムにより、自身の菌の生息密度を感知し、毒素の産生をコントロールしています。S. aureusのAgr-QSの下流で発現する毒素のσ-toxinは、マスト細胞の脱顆粒を引き起こして、Th2炎症を誘発ます。PSMαは、表皮バリア破壊を引き起こし、ケラチノサイトからのアラーミンであるIL-1α及びIL-36α等のサイトカインの放出を誘導して、IL-17依存性の皮膚炎を惹起して、アトピー性皮膚炎の皮膚症状を悪化させます。また、Agr-QSの下流のSspAは、神経系のPAR1受容体を介して、痒みを誘発させます。つまり、S. aureusは、Agr-QSの活性化により、アトピー性皮膚炎の重要な3病態とされる、Th2免疫と表皮バリア破壊、痒みの全てを悪化させます。
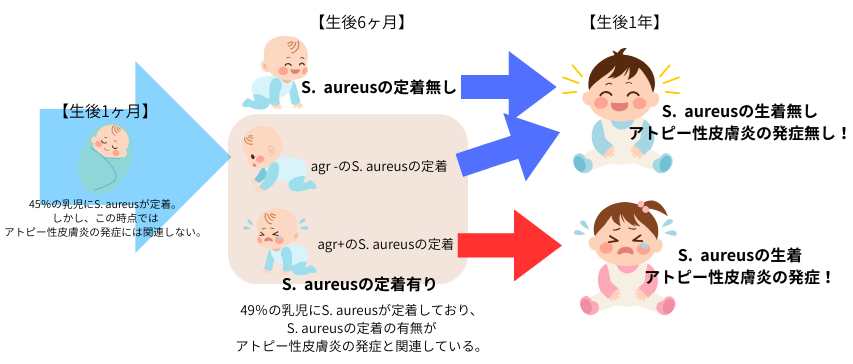
何でこんな事態が発生してしまったのかは、未だ詳しい事は分かってはいませんが、論文によれば、生後6ヶ月の時点で、S. aureusが皮膚に定着している乳児ではアトピー性皮膚炎の発症リスクが有意に高くなっています。
■尋常性乾癬
これまで、尋常性乾癬(美容通信2019年9月号)(美容通信2026年3月号)(美容通信2008年4月号)の病変部では、細菌の多様性が低下し、Streptococcus属やStaphylococcus属の増大、Cutibacterium属の減少、真菌(特に、Candida albicans)の増大が指摘されています。
微生物が乾癬を増悪させるメカニズムとしては、乾癬部では、Streptococcus pyogens由来のスーパー抗原を認識するT細胞の割合が増えているからとか、C. albicans由来の抗原により誘導されるIL17産生CD4+エフェクターT細胞の増加と、好中球の皮膚浸潤によるneutrophil extracellular traps(NETs)形成が皮膚炎を増悪させるとか、S. aureusによるTh17炎症の亢進、Malassezia属による好中球の活性化等が考えられています。
■尋常性痤瘡(ニキビ)
尋常性痤瘡(ニキビ)(美容通信2026年6月号)(美容通信2023年8月号)の発症や増悪には、ホルモンバランスや脂質代謝の異常による皮脂の過剰産生や角化異常と、C. acnesを中心とした細菌の増殖とそれによる炎症の誘発を中心に、複雑に様々な因子が関与して発症します。
尋常性痤瘡の患者さんでは、菌叢を構成する細菌の種類が変化しているというより、同じC. acnesでも、より活性が高くて病原性の高い株の割合が増加している事が知られています。この株は、バイオフィルムを形成する能力に長け、更にはChristie-Atkins-Munch-Petersen(CAMP)因子の発現や活性酸素の生成を通して、宿主の炎症性サイトカインを誘導し、ニキビを増悪させます。
皮膚バリアの恒常性維持機構
表皮は、角化細胞が層状に重なった角化型重層扁平上皮組織で、基底層で増殖した角化細胞が、有棘層、顆粒層、角層へと分化しながら上昇して、形成されます。
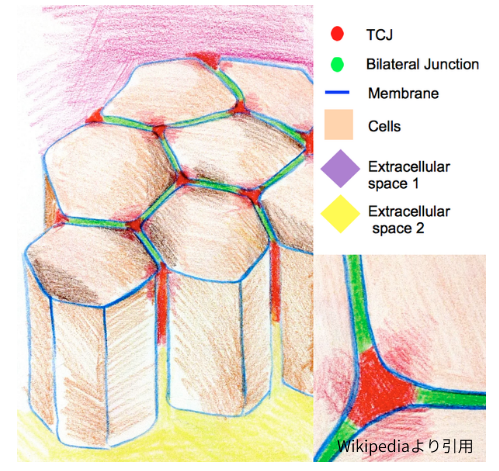 表皮最外層の角質、表皮顆粒層の角化細胞間に存在するタイトジャンクションは、皮膚のバリアとして機能します。顆粒層の角化細胞は表層から順にSG1、SG2、SG3細胞と名前が付いていますが、タイトジャンクションはSG2細胞間に存在しています。
表皮最外層の角質、表皮顆粒層の角化細胞間に存在するタイトジャンクションは、皮膚のバリアとして機能します。顆粒層の角化細胞は表層から順にSG1、SG2、SG3細胞と名前が付いていますが、タイトジャンクションはSG2細胞間に存在しています。
タイトジャンクションは、4回膜貫通蛋白質のClaudin-1が細胞膜上で重合して形成されるTJストランドと呼ばれる構造を作り、隣接する細胞のTJストランド同士がジッパーの様に結合して、細胞膜間を密着させます。その結果、細胞間を通り過ぎようとする物質の移動が制限されます。皮膚最外層の角層は、死んだ角化細胞と角層間脂質によって構成され、乾燥や物理的な損傷から私達の体を守っています。角層は、SG1細胞が、炎症を起こさずに、核・ミトコンドリア等のオルガネラが消失する特殊な細胞死(コルレオトーシス)を起こし、数層~数十層の死細胞が堆積する事で形成されます。死体の集積にも拘わらず、角層は自身の厚さを保つ機序や皮膚バリア機能を有しており、角層の恒常性の維持に寄与しています。
角化細胞の機能的細胞死(コルレオトーシス)
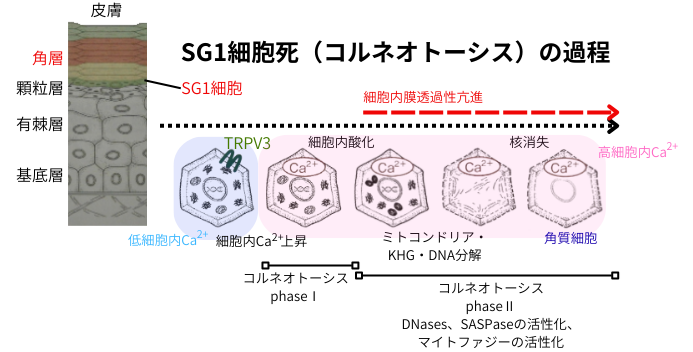 細胞死には、アポトーシス、ネクローシス等の多様な形態が存在しますが、死後に残された、所謂ご遺体である細胞体には、核やミトコンドリア等の多くの起炎物質が残っている為、不要なものは、通常はお掃除屋担当の貪食細胞によって処理されます。しかし、角化細胞は、炎症を引き起こす事なくオルガネラを消失させ、表皮顆粒層にて細胞死を遂げます。残された所謂ご遺体である細胞体は、バリア機能を有する角層の形成に再利用されます。全く、究極のサステナブル!です。右図は、このレオンも真っ青な完璧なお掃除屋のお仕事ぶりを図示したものですが、細胞内Ca2+が約1時間上昇した後(phaseⅠ)に、細胞内Ca2+が高いまま酸化する(phaseⅡ)と言う、2つのphaseから構成されています。phaseⅡでは、DNases(DNaseaIL2、DNase2)やSASPase、マイトファジーが活性化し、オルガネラが炎症を起こす事なく消失し、角質細胞に昇華!します。
細胞死には、アポトーシス、ネクローシス等の多様な形態が存在しますが、死後に残された、所謂ご遺体である細胞体には、核やミトコンドリア等の多くの起炎物質が残っている為、不要なものは、通常はお掃除屋担当の貪食細胞によって処理されます。しかし、角化細胞は、炎症を引き起こす事なくオルガネラを消失させ、表皮顆粒層にて細胞死を遂げます。残された所謂ご遺体である細胞体は、バリア機能を有する角層の形成に再利用されます。全く、究極のサステナブル!です。右図は、このレオンも真っ青な完璧なお掃除屋のお仕事ぶりを図示したものですが、細胞内Ca2+が約1時間上昇した後(phaseⅠ)に、細胞内Ca2+が高いまま酸化する(phaseⅡ)と言う、2つのphaseから構成されています。phaseⅡでは、DNases(DNaseaIL2、DNase2)やSASPase、マイトファジーが活性化し、オルガネラが炎症を起こす事なく消失し、角質細胞に昇華!します。
皮膚バリアの最前線である角層
角化細胞がコルネオトーシスを経て角質細胞となり、そして数層から数十層の角質細胞(死細胞)が重なり合う事で、角層が形成されます。
■角層pH三層構造
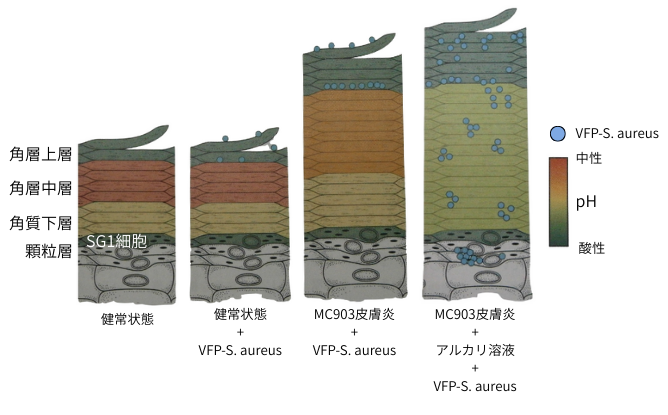
SG1細胞は角質細胞となった後、弱酸性から酸性、中性へと、段階的に分化し、健常状態では体の部位に拘わらず、あらゆる角層でpH三層構造が維持されています。この三層構造の形成には、正常に機能するタイトジャンクションの存在が不可欠とされています。
- 角層上層は、外部環境に応じてpHが変動
角層中層及び下層のpHは一定に保たれていますが、上層は外部環境に応じてpHが変動します。
- 角層中層は、黄色ブドウ球菌の侵入を防ぐバリアとして機能
角層中層は、黄色ブドウ球菌の侵入を防ぐバリアとして機能しています。
上図を見て下さい。健常皮膚にVFP発現黄色ブドウ球菌VFR-S. aureusを塗布したところ、VFR-S. aureusは角層上層表面及び角層上層と中層の境界面に定着しました。MC903を塗布して皮膚炎を起こした角層pHマウスにVFR-S. aureusを塗布した場合も、VFR-S. aureusは、角層上層と中層の境界面に定着し、水平方向に増殖しただけでした。しかし、アルカリ溶液を塗布して角層を中性化すると、VFR-S. aureusは角層全体及び顆粒層まで侵入してしまいました。
- 角層pH三層構造の生物学的意義
角層の厚みは、角化細胞が産生する蛋白質分解酵素のカリクレイン関連ペプチターゼ(KLK)が、角質細胞の接着分子を分解し、角化細胞を剥離(=落屑)させる事で、一定に保たれています。KLKの最適pHは7.8で、酸性下では酵素活性が低く、更には、KLKに結合してKLKの酵素活性を抑制する因子である、リンパ上皮Kazal型関連阻害因子(LEKT1)は、酸性の環境下でKLKから外れる事が知られています。ですから、角層pH三層構造に於いては、KLKは弱酸性を呈する下層で、LEKT1により不活性化されています。酸性の中層では、LEKT1は外れはしますが、KLKは不活性化したままの状態です。中性の上層に至って、初めてKLKが活性化して、角化細胞が剥離します。
つまり、角層は単に死んだ角化細胞が堆積した層ではなくて、異なるpHを持つ三層構造を形成しており、これは、皮膚表面でのみ落屑を促進させ、角質の厚みを一定に保つのに適した構造です。
タイトジャンクションとランゲルハンス細胞との相互作用
表皮には、角層とタイトジャンクションによる物理的な皮膚バリアに加え、ランゲルハンス細胞と言う免疫機能を有する皮膚バリアが存在します。
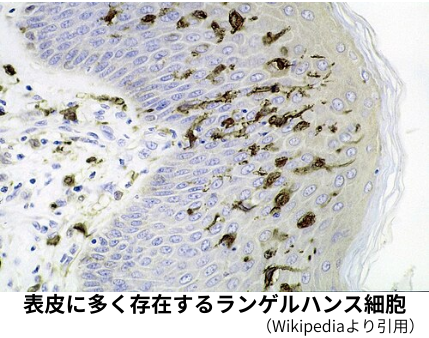
ランゲルハンス細胞は、表皮に存在する樹状細胞の一つで、発見者であるドイツの医学者パウル・ランゲルハンスにちなんで名付けられました。骨髄で造られ、表皮有棘層に存在する樹状細胞であり、表皮全体の細胞数の2〜5%を占めています。
樹枝状の突起がありますが、健常状態では、その先端はタイトジャンクションバリアの内側に大人しく留まっています。しかし、物理的な刺激やIL-1、TNF-α等のサイトカインに暴露されると、俄然、目を覚まし、樹状突起を伸ばして、タイトジャンクションバリアとドッキングしたり、タイトジャンクションバリアを超えて角層の底面にまで達します。ランゲルハンス細胞は、樹状突起の先端から抗原を取り込み、約48時間で表皮から真皮に移動し、リンパ管を経て、リンパ節に至ります。そこで、T細胞に抗原提示を行い、Th2免疫を誘導します。特筆すべき事としては、抗原の取込みの際に、SG2細胞とランゲルハンス細胞の間に、新たにタイトジャンクションバリアが形成され、バリアに漏れがないようにしっかりとガードする仕組みが出来るって事。「全く、凄い!」の一言ではあります。
タイトジャンクションと感覚神経との相互作用
表皮内に存在する感覚神経は、感覚知覚に於いてと~っても重要で、外部からの刺激に応答して脳に信号が送られます。健常皮膚では、この表皮神経の終末は、タイトジャンクションの下で伸びたり縮んだりを頻繁に繰り返しており、新しく出来たタイトジャンクションに先端がぶつかりそうになると、頭を引っ込めて、タイトジャンクションを超えてまで遠征を試みようとしません。しかし、炎症が起こると、この慎ましやかな忖度の機構が崩れ、神経末端はタイトジャンクションの外側にまで枝を伸ばしてしまいます。この食み出した枝の部分が、感覚神経の異常な活性化と痒みの引き金になると考えられています。
タイトジャンクションは、皮膚バリアの完全性と恒常性を維持する、重要な制御中枢なんですね。
セラミドによる皮膚透過性バリアの形成
皮膚のバリアは生体防御に極めて重要であり、怪我や火傷による損傷は、感染症のリスクを著しく高めてしまいます。脂質は親水性の物質の透過を防ぎ、密にパッキング出来る特性を有する事から、バリア形成に適した分子です。中でも、セラミド(美容通信2015年2月号)は、化学的に安定、且つ、強固な脂質-脂質間相互作用を形成し得る構造を有しており、皮膚バリア形成脂質として非常に優れた特性を有しています。私達の表皮角質層に存在するセラミドは、実に多種多様であり、23クラスと1500を超える分子種が存在していますが、逆に言えば、強固な皮膚バリアの形成には、それほどまでの多彩なセラミドが必要である事を示しています。
アトピー性皮膚炎では皮膚のバリア機能低下により、アレルゲンが侵入しやすい状態になっており、バリア機能の低下にセラミド量の減少や組成変化が関わっています。また、アシルセラミドヤ結合型セラミドは、皮膚バリア形成に特化したセラミドの代表格ですが、この合成に係る遺伝子が変異してしまうと、先天性魚鱗癬が発症します。
皮膚バリアに重要な角質層構造体とセラミド
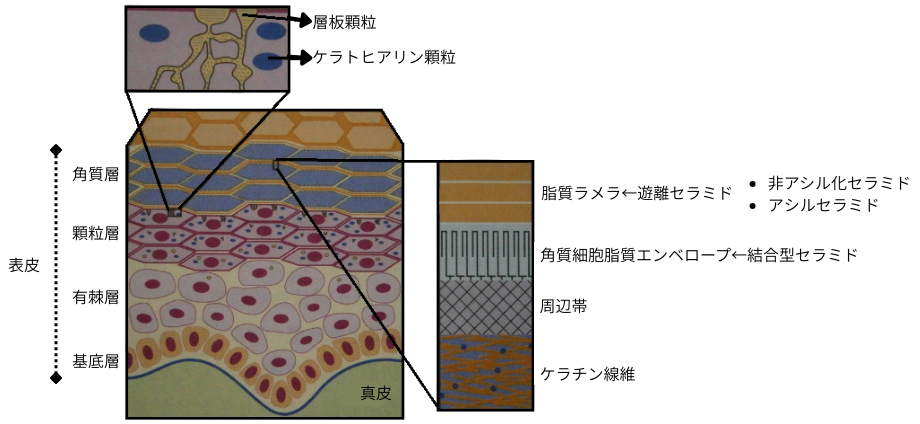
セラミドは、顆粒層に於いて活発に合成され、極性基が付加された状態で、一旦は層板顆粒内に蓄えられます。層板顆粒とは、角質層セラミドの前駆体となるグルコシルセラミド、スフィンゴミエリン等が蓄えられた構造体で、以前は独立した顆粒と考えられていましたが、最近では、トランスゴルジネットワークから伸びたチューブ状の構造体と考えられています。この層板顆粒への輸送を担うのが、ABCトランスポーターABCA12です。その後、顆粒層ケラチノサイトが角質細胞(角質層ケラチノサイト)に変化する過程で、内包されたグルコシルセラミド/スフィンゴミエリンの細胞外への放出と極性基の除去(セラミドへの変換)が起こります。
セラミドは、角質層に於いて皮膚バリアに重要な2つの構造体、即ち、脂質ラメラと角質細胞脂質エンベロープで構成されています。
■脂質ラメラ
脂質ラメラとは、角質細胞の細胞間に充填された脂質の多層構造体で、主要構成成分はセラミド、コレステロール、遊離脂肪酸です。変異によってABCA12の機能が失われると、グルコシルセラミド/スフィンゴミエリンが層板顆粒へ輸送されず、角質層内での脂質ラメラ形成が大きく損なわれます。
■角質細胞脂質エンベロープ
角質細胞脂質エンベロープは、角質細胞を覆う形質膜様の構造体で、構成成分は角質細胞表面の蛋白質(周辺帯の蛋白質)と共有結合した特殊な結合型セラミドです。顆粒層ケラチノサイトが角質細胞へと分化する過程で、通常の脂質二重層からなる形質膜は、角質細胞脂質エンベロープに置き換わります。結合型セラミドは、化学的/物理的に安定、且つ、界面活性剤や一般的なリパーゼに対し耐性があります。また、脂質ラメラ中のセラミドと強く相互作用して、脂質ラメラの角質細胞膜上の安定化に寄与します。
セラミドの多様性
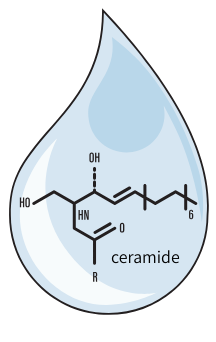 セラミドは、長鎖塩基と脂肪酸がアミド結合した構造です。一般的なセラミドはこの2本の疎水鎖のみで構成された非アシル化セラミドだけですが、私達の表皮角質層に存在するセラミドは、実に多種多様であり、23クラスと1500を超える分子種が存在しています。つまり、強固な皮膚バリアの形成には、多彩なセラミドの存在が必要なのです。
セラミドは、長鎖塩基と脂肪酸がアミド結合した構造です。一般的なセラミドはこの2本の疎水鎖のみで構成された非アシル化セラミドだけですが、私達の表皮角質層に存在するセラミドは、実に多種多様であり、23クラスと1500を超える分子種が存在しています。つまり、強固な皮膚バリアの形成には、多彩なセラミドの存在が必要なのです。
表皮のセラミドには遊離型と結合型があります。遊離型セラミドには、一般的な非アシル化セラミドと、この脂肪酸の部分のオメガ末端にリノール酸が付加したアシルセラミドがあり、これ等は脂質ラメラを構成しています。結合型は、蛋白質と共有結合しており、角質細胞脂質エンベロープを構成しています。私達の角質層セラミド中の割合は、非アシル化セラミドが77%、アシルセラミドが9%、結合型セラミドが14%を占めています。アシルセラミドは量的には決して多くはないですが、脂質ラメラの中で伸びた構造を取る事で、層と層の間を跨って存在し、ラメラ構造の安定化に極めて重要なセラミドです。
アトピー性皮膚炎や乾癬、乾燥肌に於けるセラミドの組成変化
アトピー性皮膚炎のみならず、乾癬や乾燥肌では、程度は異なるものの、セラミドの組成変化、つまり、NP、NH、EOS、EOP、EOHセラミドの減少と、NS、ASセラミドの増加が起こる事が知られています。NP、NHは非アシル化セラミドで、これ等の減少は水素結合による脂質-脂質間相互作用の減弱を意味します。また、EOS、EOP、EOHは、何れも、脂質ラメラ構造の安定化に寄与するアシルセラミドですから、この減少は脂質ラメラの不安定化を意味します。
メラノソームの形成と輸送
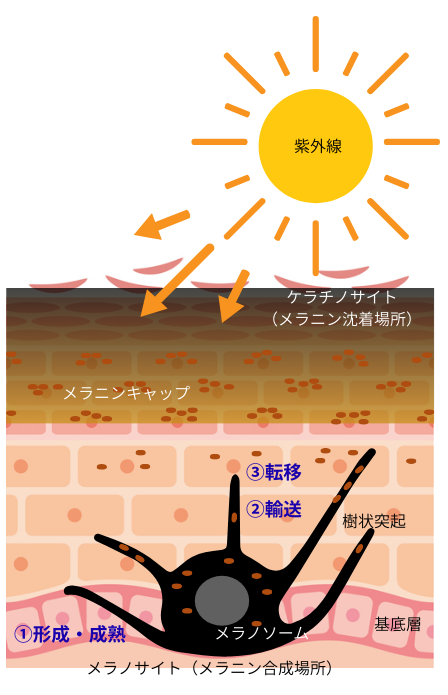 メラニンは、私達の皮膚や髪の毛の色合いを決める色素で、皮膚の基底層や毛球に存在するメラノサイトで合成されています。メラノサイトは、リソソームと一部共通の性質を有するメラノソームと呼ばれる特殊な細胞小器官を有し、その内部でメラニンの合成・貯蔵の役割を担っています。
メラニンは、私達の皮膚や髪の毛の色合いを決める色素で、皮膚の基底層や毛球に存在するメラノサイトで合成されています。メラノサイトは、リソソームと一部共通の性質を有するメラノソームと呼ばれる特殊な細胞小器官を有し、その内部でメラニンの合成・貯蔵の役割を担っています。
紫外線等の紫外線等の刺激によって、表皮のメラノサイトは活性化され、メラノソームの形成・成熟が核周辺で促進されます。メラノソームの形成は段階的に行われ、形態学的に4つのステージに分類されています。黒く成熟したメラノソームは、細胞骨格に沿って細胞辺縁部(樹状突起の先端部)まで輸送された後、隣接するケラチノサイトに受け渡されます。ケラチノサイトに取り込まれたメラノソームは、最終的に核の上部まで輸送され、メラニンキャップを形成し、有害な紫外線から核(DNA)を保護します。この様に、メラノサイトの合成場所(メラノサイト)と沈着場所(ケラチノサイト或いは毛母細胞)が全く異なる為、皮膚や毛髪の暗色化には、適切なメラノソームの形成、輸送、転移が必須となります。この何れかの過程が損傷されると、白皮症に代表される遺伝的な病気が発症します。
しかし、ケラチノサイトでのメラニンの過剰な沈着は、シミやそばかすの原因となりますが、メラノソームの輸送や分解の遅延との関係は未だ分かってはいません。これが解明されると、将来的には、シミやそばかすの予防や治療(美容通信2013年12月号)(美容通信2003年6月号)に繋がると考えられています。
皮膚の伸縮
皮膚の力学的な特性は、大まかに細胞外マトリックスが既定しています。そのなかでも、引っ張り強度は線維性コラーゲン(膠原線維)が付与しており、幾ら引っ張ったとしても、頑として抗い、伸び縮みしません。これに対し、伸縮性を担うのは弾性線維で、ゴムの様に2倍に引き伸ばしても、元に戻ると言う性質があります。生理的な力の大きさで張力が掛かる間は弾性線維の特性が、それ以上の張力が掛かると線維性コラーゲンの特性が前面に出て来るように、敢えて線維性コラーゲンを弛ませて織り込んでいます。線維化を起こした組織では、線維性コラーゲンが過剰に作られ、最初から線維性コラーゲンに張力が掛かる様になり、硬く、進展性が欠如した状態になっています。この様な線維化は、皮膚だけに留まらず、肺や心臓、肝臓等の様々な臓器に於いて起こり、様々な疾患の原因となります。
弾性線維は、半減期は70年以上と、極めてターンオーバーが遅い組織で、基本的に、加齢や紫外線により壊れた皮膚の弾性線維が再生する事はないと考えられています。加齢した皮膚の露光部で生じる日光弾性線維症では、エラスチンの過剰な沈着は認めますが、正常な弾性線維としての形と機能は有しておらず、皮膚は弛むしかありません。皮膚以外でも、弾性線維の劣化・分解は、肺気腫や動脈中膜効果の直接的な原因となります。
弾性線維の構成蛋白質:エラスチンとミクロフィブリル
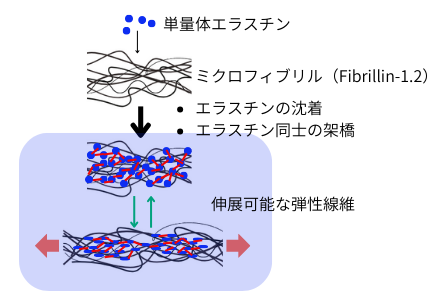 右図は、弾性線維形成の概略を示した図です。弾性線維の主体は架橋されたエラスチン蛋白質ですが、その形成過程では、①単量体エラスチンがミクロフィブリルに沈着し、②エラスチン同士がリシルオキシターゼによって架橋されると言うプロセスが取られます。
右図は、弾性線維形成の概略を示した図です。弾性線維の主体は架橋されたエラスチン蛋白質ですが、その形成過程では、①単量体エラスチンがミクロフィブリルに沈着し、②エラスチン同士がリシルオキシターゼによって架橋されると言うプロセスが取られます。
皮膚の弾性線維は真皮で作られますが、表皮との境界では、表皮に垂直な細い線維として、より深部の真皮では体表面に平行に走行する太い線維として存在しています。
エラスチンをミクロフィブリル上に沈着させる糊:Fibulin-5とLTBP-4
Fibulin-5は、エラスチンと結合してそのコアセルベーションを促進し、ミクロフィブリル上への沈着を増加させる糊のような存在です。このFibulin-5をミクロフィブリル上に誘導しているのが、Latent TGFβ-binding protein(LTBP)-4って奴で、ミクロフィブリル上に共局在しています。
エラスチンを架橋するツール:リシルオキシダーゼ(LOX)とFibulin-4
LOXは、リジン残基の側鎖を酸化して、反応性の高いアルデヒドに変化させる酵素で、これにより出来たアルデヒドが、近隣のリジン残基やアルデヒドとべたべたくっ付いて共有結合を作り、架橋が形成されます。LOXは、エラスチンだけでなく、コラーゲンの架橋酵素でもあり、細胞外マトリックスの強度を規定する上で極めて重要な酵素です。因みに、LOXノックアウトマウスでは、コラーゲンとエラスチンの架橋が阻害されているので、大動脈の破裂、横隔膜の破裂等で、生後直ぐに死んでしまいます…。
Fibulin-4は、LOX産生細胞の小胞体、若しくは細胞外から取り込まれて、ゴルジ体に輸送されます。LOX前駆体は、ゴルジ体内で、銅イオントランスポーターATP7aから銅イオンを受け取りますが、この際、Fibulin-4との結合が前提となります。銅イオンの存在下で分子内架橋LTQが形成され、LTQが酵素活性の中心になります。分泌後は、プロドメイン及びそこに結合したFibulin-4は切断され、活性型LOXが出来ます。つまり、LOX活性化になくてはならないのが、Fibulin-4です。
加齢皮膚と日光弾性線維症に於ける弾性線維形成蛋白質
加齢皮膚でみられる日光弾性線維症では、真皮浅層にエラスチンの過剰な沈着が認められ、少なくとも加齢した皮膚の真皮に於いても、エラスチンの発現能はある事はありますが、だからと言って、正常な弾性線維を生成出来る訳ではありません。日光弾性線維症では、誘導灯のLTBP-4が、何故かは分かりませんがいなくなってしまい、これまた何で過剰発現してしまったのか解明されてはいませんが、過剰発現してしまったエラスチンが、交通整理のおじさんがいないが故に、右往左往した挙句に、無秩序な大きな団子状の塊をそこかしこに作ってしまいます。
皮膚に於ける力学的刺激と創傷治癒に与える影響
 重力や大気圧を始めとする種々の力学的刺激(メカニカルストレス)は、日常の生活の中で自然に存在するものであり、人体の構造や機能に大きな影響を及ぼしています。例えば、重力は骨や筋肉の発達を促進し、体を支える役目を果たしています。大気圧は、呼吸器や循環器系の正常な機能を維持する為に欠かせない要素です。この様に、地球環境に於ける力学的な刺激は、生物の適応や進化、更には日々の健康状態にも密接に関連しています。
重力や大気圧を始めとする種々の力学的刺激(メカニカルストレス)は、日常の生活の中で自然に存在するものであり、人体の構造や機能に大きな影響を及ぼしています。例えば、重力は骨や筋肉の発達を促進し、体を支える役目を果たしています。大気圧は、呼吸器や循環器系の正常な機能を維持する為に欠かせない要素です。この様に、地球環境に於ける力学的な刺激は、生物の適応や進化、更には日々の健康状態にも密接に関連しています。
皮膚もその例外ではなく、常に力学的刺激を感受しており、その影響によって皮膚の構造や機能が維持されています。具体的には、張力や圧力を受ける事で、細胞外基質の産生や細胞の活動が調整される等、細胞から組織・臓器に至るまで、広範囲に亙る適応反応が引き起こされます。
皮膚と力学的刺激
皮膚には、その力学的特性を規定する3つの主要な蛋白質があります。①膠原線維を構成するコラーゲンは、皮膚の強度と安定性を担当し、主に張力に対する抵抗する役割があります。これに対し、②グルコサミノグリカンは、細胞外基質中で水分を保持する事で圧力に抵抗し、皮膚の体積維持や弾力性に寄与しています。③弾性線維を構成するエラスチンは優れた伸展性を持ち、皮膚が伸縮や変形に対して柔軟に適応が出来る様にしています。これらの3つの蛋白質は、夫々異なる特性を持ちながらも、相互に影響を及ぼし合う事で、皮膚の外的な力学的刺激に対する適応力を構成しています。ですから、これ等の蛋白質のバランスが崩れると、皮膚の力学的特性が低下し、組織の脆弱性や瘢痕形成等の病態に繋がります。
体の部位によって皮膚の構造が異なるのは、皮膚が部位特有の力学的刺激を受け、それに適応した結果でもあります。例えば、上眼瞼の皮膚は、眼を強く開いたり閉じたりしても大きな張力が掛からない様に、コラーゲンの産生が少なく、結果として真皮が非常に薄くなっています。反対に、上半身の胸部や背部の皮膚は、腕を振り回す等の上肢の動作に伴って、強い張力を受けます。この様な力学的な刺激に対応する為に、真皮は厚く、コラーゲンが豊富です。また、急激にデブ化したり妊娠により伸展するお腹や、常に伸展が伴う大関節である肘や膝等では、エラスチンの分布が多くなっています。掌や足の裏の様に強い圧力が掛かる部位では、真皮内のグリコサミノグリカンが相対的に多くなっています。
■皮膚障害
例えば、切腹で腹を切ったり、酔っ払って転倒して机の角にぶつかったりすると、ぱかっと傷が開きます。皮膚のコラーゲン線維が物理的に断裂すると、通常皮膚が保っている内在的な張力に対する抵抗力が失われる為です。皮膚が損傷されると、本来の鎧兜として役割を果たす事が出来ず、外部からの力学的刺激に対し、大切な内臓を守れません。
■皮膚の創傷治癒
皮膚の創傷治癒(美容通信2004年5月号)とは、内在的及び外因性の力学的刺激に対抗し得る盾を、もう一度再構築する為の過程です。刃物で抉り取られてしまった皮膚の欠損部分は、肉芽組織って名前の、膠原線維からなる真皮もどきで充填されます。この肉芽組織では、先ず、筋線維芽細胞と共にⅢ型コラーゲンが増殖し、欠損部の収縮及びサイズの縮小に寄与します。その後、表皮細胞が増殖して移動し、上皮化が完了します。これにより、炎症が減少し、Ⅲ型コラーゲンが減少する一方で、Ⅰ型コラーゲンの割合が増え、瘢痕が成熟化に向かいます。
この過程で、肉芽組織からなる真皮様組織が、一時的な硬化を示します。この様な状態では、体の動きに合わせて傷に緊張が掛かっても、凝り固まってしまっている膠原線維では伸展が出来ず、張力を逃す事が出来ませんから、もろに被害を被ってしまいます。こうなると、小さな諍いであっても、そこに火に油を注ぐ様なものですから、炎症は増悪し、道を踏み外して肥厚性瘢痕の道に走る切っ掛けになります。更に、強い外力が続けば、隣接する周囲の皮膚にも過剰な張力が掛かり、血管透過性が亢進し、炎症が周囲の正常な皮膚まで巻き込んだ激烈なケロイド(美容通信2017年11月号)抗争に発展してしまいます。
メカノバイオロジーとメカノセラピー
用語の説明になりますが、正常、異常に拘わらず、創傷治癒過程に関与する力学的刺激の役割や、細胞が力学的刺激を感じる仕組みを研究する学問がメカノバイオロジー。メカノバイオロジーの考え方を応用して、メカニカルストレスを敢えて加えたり除いたりして、疾患を治療する事をメカノセラピーと言います。後述する、過度な力が掛かっている炎症性瘢痕に対し行うz形成術は、力を弱めるメカノセラピーですし、また、難治性潰瘍に対して行われる陰圧閉鎖療法は、力を加えるメカノセラピーです。
メカノセンサーとは、細胞の力学的刺激を感じる構造の事で、例えば、細胞膜にあるカルシウムイオン(Ca2+)チャネルや、ATPへミチャネル、インテグリン等の分子、更には細胞骨格であるアクチンフィラメント等があり、これ等が物理的な力を化学的信号に変換する役割を果たしています。
メカノセンサーが力学的刺激を感知すると、細胞内の複数のシグナル伝達経路が活性化されたり、逆に抑制されます。具体的なシグナル伝達経路としては、MAPキナーゼ経路、P13キナーゼ/AKT経路、RhoA/ROCK経路、YAP/TAZ経路等があり、これ等の経路は、細胞の増殖、分化、移動、アポトーシス等多岐に亘る細胞応答を制御しています。例えば、細胞が張力を受けると、YAP/TAZ経路が活性化されて遺伝子発現が促進され、細胞の形態や機能が変化します。更には、これ等のシグナル伝達経路の活性化や抑制は、転写因子の活性化を通じて、遺伝子発現の調節に繋がります。つまり、力学的刺激によって、特定の遺伝子のプロモーター領域が活性化され、必要な蛋白質の合成が増加したり、他の遺伝子の発現が抑制されたりします。この様に、細胞は環境の物理的な変化に適応し、適切な生理学的な応答を行う…実に、臨機応変。と~っても賢い存在なのです。
力学的な刺激によって変化する複数のシグナル伝達経路全体を総称して、メカノシグナル伝達経路と呼びます。この経路は、細胞が外部から受ける物理的な力を、生理学的な信号に変換し、細胞の機能や挙動を調節する重要なメカニズムであり、中でも、力学的な信号を受け取って細胞内での変化を引き起こす一連の過程を、メカノトランスダクションと言います。
メカノセラピーの応用は、将来的には、細胞が自然に力学的な刺激を受けた際に発現する一連の生物学的反応を人工的に再現する治療薬「メカノピル」の開発に繋がると考えられています。また、線維症や癌、再生医療、美容医療分野に於いても大きな可能性を秘めており、特に、老化により弾力性を失った皮膚に対して力学的な刺激を加える事で、コラーゲンやエラスチンの生成を促し、皮膚の若返りやハリの回復に繋がるものと思われます。
 因みに、右図は、江戸時代の力士の出で立ちです。江戸時代には関所を通行するには通行手形が必要でしたが、力士はその大きく筋肉質な体つきから、他の者が関所破りの目的で力士に変装するのは困難!であるとされ、通行手形が無くとも通行出来ました。力士の他に、通行手形がなくても通行可能だったのは旅の芸人だけでですが、彼らは芸を見せて関所の役人を納得させる必要がありました。江戸幕府は1827年、大名抱えの力士は武士とするが、それ以外は浪人であるという見解を示しました。召し抱えられた力士以外は全て浪人とする解釈は多少強引とも言えなくもない(笑)ですが、これにより、農民や町人であっても、力士にさえなれれば、武士・浪人になれたんです。
因みに、右図は、江戸時代の力士の出で立ちです。江戸時代には関所を通行するには通行手形が必要でしたが、力士はその大きく筋肉質な体つきから、他の者が関所破りの目的で力士に変装するのは困難!であるとされ、通行手形が無くとも通行出来ました。力士の他に、通行手形がなくても通行可能だったのは旅の芸人だけでですが、彼らは芸を見せて関所の役人を納得させる必要がありました。江戸幕府は1827年、大名抱えの力士は武士とするが、それ以外は浪人であるという見解を示しました。召し抱えられた力士以外は全て浪人とする解釈は多少強引とも言えなくもない(笑)ですが、これにより、農民や町人であっても、力士にさえなれれば、武士・浪人になれたんです。
■肥厚性瘢痕とケロイドの治療
肥厚性瘢痕やケロイドの治療は、そもそもの原因となった炎症性瘢痕に力が掛かり難い状況を作る事です。形成外科の面目躍如ではありませんが、ケロイドを切除し、z形成術等でジグザグに縫合して張力を分散させるのも一案ですし、薬(副腎皮質ホルモン)の力を借りて炎症を抑え込んだり、放射線照射を併用して、非機能的な毛細血管を叩き、炎症を軽減させる治療法もあります。
■創傷治癒遅延と力学的刺激
糖尿病や免疫抑制状態では、創傷治癒は遅延します。糖尿病患者さんでは、高血糖により、血流障害や神経障害が発生します。血流障害は、酸素や栄養素の供給不足を招き、創傷治癒を遅延させます。また神経障害によって、神経原性炎症が十分に起こらず、炎症反応や免疫細胞の動員が不十分になります。更には、高血糖状態では白血球の機能低下や接着分子の分泌が低下し、感染リスクが増加します。コラーゲン合成の阻害等により、組織修復が妨げられます。これ等の要因が複合的に作用し、糖尿病患者さんでは体表面の創傷治癒が著しく遅延します。免疫抑制状態では、免疫細胞の機能低下により、感染の防御が不十分になるだけでなく、炎症反応が適切に起こらず、サイトカインや成長因子の分泌が減少します。これにより、線維芽細胞の活性化やコラーゲンの合成、血管新生が妨げられ、組織修復が遅れます。また、免疫抑制により、細胞の増殖や移動が阻害される為、創傷部位の再生が円滑に進まず、全体として創傷治癒が遅延します。
この様な状態では、創部に適切な張力が掛からない状態が持続し、通常なら想定する必要すらなかった力学的な刺激に対しても、制御不能に陥ってしまいます。その結果、細胞の遊走やコラーゲン合成が阻害されて、組織修復が遅れる為に、創傷治癒が著しく遅延し、慢性潰瘍・難治性潰瘍になります。
■創傷治癒促進を目的とした力学的刺激の負荷
陰圧閉鎖療法とは、慢性潰瘍や難治性潰瘍部分を陰圧で吸引して、敢えて力学的刺激を加える事で、細胞の活性化を図る治療方法です。傷の血管新生や膠原線維産生が促進される事で、良好な肉芽組織が形成されて、上皮化が促されます。更には、創面の余計な液体や感染物質を除去して、傷環境を清潔に保つ効果も期待出来るだけでなく、疼痛の軽減、患者さんの快適性の向上にも寄与してくれるので、患者さんが「もう、めんどいから、嫌だ。放っておいてくれ!」と治療を途中で投げ出してしまう事がなくなります(←100%ではありませんが!)。
一次求心性痒み神経
 痒みとは、皮膚や粘膜を引っ搔きたくなる様な不快な感覚の事を言います。皮膚表面に貼り付いた有害物を取り除く為の引っ掻き行動を誘発する、生体防御的な感覚です。一般的に痒みは、皮膚に於ける一次求心性感覚神経への刺激を起点として、そのシグナルが脊髄後角及び脳へ伝達されて生じます。
痒みとは、皮膚や粘膜を引っ搔きたくなる様な不快な感覚の事を言います。皮膚表面に貼り付いた有害物を取り除く為の引っ掻き行動を誘発する、生体防御的な感覚です。一般的に痒みは、皮膚に於ける一次求心性感覚神経への刺激を起点として、そのシグナルが脊髄後角及び脳へ伝達されて生じます。
皮膚炎による一次求心性感覚神経の変化
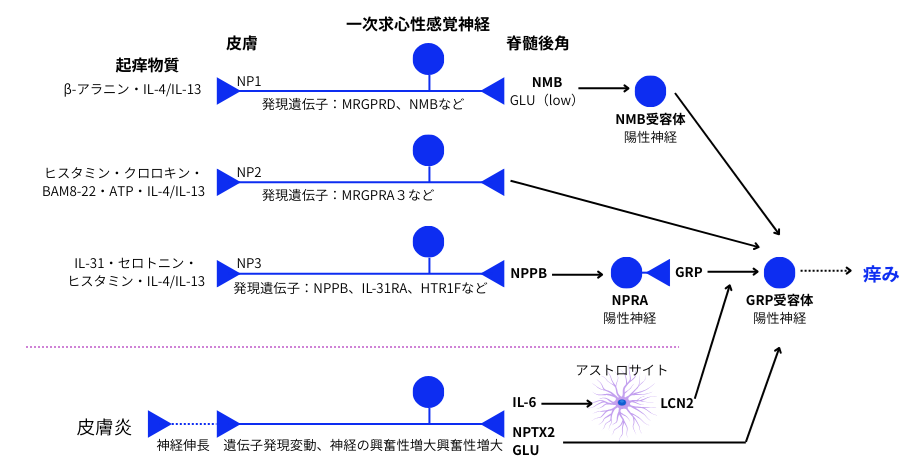
起痒物質に反応する一次求心性感覚神経は、主にNP1/2/3神経サブセットです。
- NP1神経サブセット:NP1神経は、MRGPRDの選択的な発現を特徴とし、一次求心性神経の約20%を占める集団です。MRGPRDは、β-アラニンによって活性化され、痒みを誘発します。NP1神経は、脊髄後角の神経終末からNMBを放出し、NMB受容体陽性及びGRP受容体陽性神経を活性化し、痒みを引き起こします。
- NP2神経サブセット:MRGPRA3を選択的に発現し、一次求心性神経の約4~5%を占めます。MRGPRA3は、抗マラリア薬クロロキンによる痒みの標的蛋白質である事が知られています。
- NP3神経サブセット:このサブセットは、起痒物質であるセロトニンの受容体HTR1Fや、脊髄後角で痒みを誘発するNPPB、慢性掻痒に重要なIL-31の受容体が、選択的に発現する特徴を有しています。IL-31は、アトピー性皮膚炎や創傷治癒に伴う痒みに関与し、前述の2023年に発売された生物製剤ミチーガ(ネモリズマブ)は、末梢神経のIL-31受容体を標的とするお注射です。
NP神経サブセットには、それ以外にも、痒みシグナルを増強するIL-4やIL-13の受容体も発現し、皮膚炎モデルの痒みへの関与が示されています。因みに、デュピクセント(デュピルマブ製剤)(美容通信2019年7月号)は、I L-4/13によるシグナル伝達を阻害し、アトピー性皮膚炎の病態に深く関与するTh2型炎症反応を抑える、世界初のヒト型抗ヒトIL-4/13受容体モノクローナル抗体(生物学的製剤)です。
L-4/13によるシグナル伝達を阻害し、アトピー性皮膚炎の病態に深く関与するTh2型炎症反応を抑える、世界初のヒト型抗ヒトIL-4/13受容体モノクローナル抗体(生物学的製剤)です。
■皮膚炎による一次性求心性感覚神経の変化
- 皮膚内での神経の伸長と退縮
皮膚バリアの機能低下による皮膚の乾燥(美容通信2003年12月号)は、痒みを誘発します。ドライスキンでは、MRGPRA3陽性神経を含む一次求心性感覚神経の自由終末が、真皮内から表皮内へと伸長・分枝化し、痒みの閾値の低下に寄与しています。この現象には、表皮角化細胞で発現する神経栄養因子が関与するだけでなく、メルケル細胞とMRGPRA3陽性神経の異常な連結が起こっており、慢性的な痒みに繋がっていると考えられています。
- 遺伝子発現及び神経活動の変化
アトピー性皮膚炎等の皮膚炎に伴い、一次求心性感覚神経の遺伝子が変化し、神経の興奮性が高まります。更に、発現増加したIL-6は、脊髄後角のアストロサイトを活性化し、産生されたLCN2がGRPシグナルを亢進させます。
皮膚温度感覚
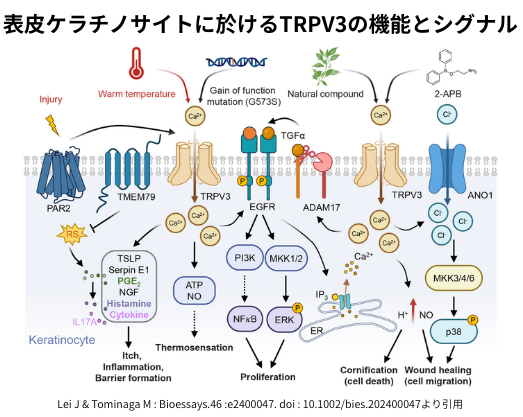
皮膚は、様々な外界からの刺激を感知します。そして、温度は、感覚神経に加えて、表皮ケラチノサイトで感知します。その温度感知に係るのが、温度感受性TRPチャンネルであり、表皮ケラチノサイトでは温かい温度を感知するTRPV3、TRPV4が主に機能します。TRPV3は、皮膚で温度を感知して、その情報を感覚神経に伝達するだけでなく、表皮ケラチノサイトの増殖や移動にも関与します。TRPV4は、皮膚のバリア機能の調節や汗の分泌等に関与します。また、TRPV3、TRPV4は、皮膚の痒みにも関わっており、創薬標的として期待されています。
感覚神経での温度感知
感覚神経で温度情報を受容する最も簡単で有効的なメカニズムは、陽イオンの流入が齎す脱分極から、電位作動性ナトリウムチャンネルを活性化させて、活動電位を発生させるものです。その陽イオンの流入を司る陽イオン透過性のイオンチャンネルの多くは、高いカルシウム透過性を有し、その中心的分子群の一つTRPイオンチャンネルです。
■TRPチャンネル
1997年に、ラット感覚神経から、哺乳類で初めて温度で活性化される分子としてカプサイシンTRPV1が発見されました。カプサイシンによる辛みは、味覚ではなくて痛みである事から、熱痛み刺激と化学物質痛み刺激を共に感知する受容体として注目を浴びました。その後、温度感受性TRPチャンネルの一群が続々と同定され、7つのサブファミリーに分けられ、うち6つのサブファミリーには27のチャンネルが存在する事が分かっています。
現在までに、哺乳類で温度感受性が報告されたTRPチャンネルは、TRPV3、TRPV4等、11あります。表皮ケラチノサイトには、主に体温近傍の温かい温度で活性化する2つの温度感受性TRPチャンネル、TRPV3とTRPV4が発現しています。
■TRPV3と皮膚の機能
 TRPV3は、表皮や毛包で特異的に発現する温かい温度で活性化するTRPチャンネルで、皮膚で温度を感知して、その情報を感覚神経に伝達するだけでなく、表皮ケラチノサイトの増殖や移動にも関与します。感覚神経では発現せずに、メントールやカルバクロールの様な天然化合物や2-APBで活性化します。急激な温度上昇では痒みを感じますが、これはTRPV3が関与しています。
TRPV3は、表皮や毛包で特異的に発現する温かい温度で活性化するTRPチャンネルで、皮膚で温度を感知して、その情報を感覚神経に伝達するだけでなく、表皮ケラチノサイトの増殖や移動にも関与します。感覚神経では発現せずに、メントールやカルバクロールの様な天然化合物や2-APBで活性化します。急激な温度上昇では痒みを感じますが、これはTRPV3が関与しています。
口腔粘膜上皮では、TRPV3が暖かい温度で活性化して上皮成長因子受容体(EGFR)が活性化し、上皮細胞の成長と増殖が促されて、創傷治癒が早く進みます。皮膚に於いても、TRPV3の活性化により、創傷治癒が温度で促進されます。私達人間のケラチノサイトでは、TRPV3を通って流入したカルシウムイオンが、カルシウム活性化クロライドチャンネルのANO1を活性化し、クロライドイオンが流入。p38のリン酸化を阻害する為に、細胞周期の期移行を促進させて細胞増殖を進めます。
■TRPV4
- 鎮痒剤の標的として
表皮ケラチノサイトに発現するTRPV4は、TRPV3の様な温かい温度による痒みではなく、セロトニンやヒスタミン、グルコシルスフィンゴシン、バイカレインによる痒みに関わっています。胆汁うっ滞の際の痒みは、リゾホスファチジルコリンの血清濃度上昇により、TRPV4が活性化されてマイクロRNA146aが放出されますが、これがTRPV1を活性化して、痒みが起こります。今や鎮痒剤界の古典的存在として知られるオイラックスは、含有するクロタミトンがTRPV4を阻害する事で効果を発揮します。
- 皮膚のバリア機能
表皮ケラチノサイトに於いて、TRPV4は細胞間接着構造を構成する蛋白質であるβカテニンとEカドヘリンと複合体を形成します。暖かい温度刺激を含めた刺激でのTRPV4の活性化は、①細胞内カルシウムイオン濃度の上昇、②低分子GTP結合蛋白質Rhoの活性促進、③細胞間接着構造の形成・成熟促進と、それらを介した表皮細胞間バリア機能の亢進に関係します。冬に皮膚が乾燥する理由の一つとして、温度低下によるTRPV4を介した皮膚表皮間バリア機能の減弱により、水分漏出が考えられています。
 因みに、右図は、Wikipediaから拝借したバナバの花です。この抽出物は、広く生活習慣病予防として販売されており、日本では、「フィリピンでは古くから”女王も手の届かぬ神木”」と喧伝されていましたが、実はフィリピンでは何処にでも生えているありふれた植物(笑)です。しかし、この葉っぱから単離されたエラグ酸誘導体には、高いTRPV4活性化作用及び表皮細胞間バリア機能増強作用が認められており、某化粧品会社の化粧水に含有されているそうな。
因みに、右図は、Wikipediaから拝借したバナバの花です。この抽出物は、広く生活習慣病予防として販売されており、日本では、「フィリピンでは古くから”女王も手の届かぬ神木”」と喧伝されていましたが、実はフィリピンでは何処にでも生えているありふれた植物(笑)です。しかし、この葉っぱから単離されたエラグ酸誘導体には、高いTRPV4活性化作用及び表皮細胞間バリア機能増強作用が認められており、某化粧品会社の化粧水に含有されているそうな。
- 発汗
熱い環境下では、局所皮膚のTRPV4が温かい温度を感知して、発汗を齎していると考えられています。
表皮幹細胞ダイナミクスから考える皮膚再生と老化
皮膚は、光老化(美容通信2003年7月号)(美容通信2003年8月号)等の外的要因と、分裂ストレス等の内的要因により、老化が進行し、外観や形態的変化として認識されるようになります。皮膚の老化としては、表皮の厚さの減少、表皮‐真皮接合部の平坦化、創傷治癒の遅延、バリア機能の低下、癌のリスク増加等、組織学的及び機能的な変化等が挙げられます。しかし、細胞や分子レベルでの皮膚老化の決定的な要因が何であるかは、未だ解明がされていません。
組織幹細胞は、組織の恒常性維持と損傷修復に働き、生涯に亘って、自己複製と分化を行う細胞です。しかし、細胞外マトリックスの加齢変化に加え、炎症やニッチ環境の変化は、皮膚幹細胞の性質を低下させ、加齢と共に徐々にその能力を喪失します。
皮膚の恒常性維持と再生を支える幹細胞システム
皮膚は、表面から表皮、真皮、皮下組織で構成される多層構造で、新陳代謝を繰り返しています。表層に位置する表皮は、4層からなり、表皮幹細胞を含む増殖細胞は深部の基底層に位置しています。表皮と真皮の境界部にある基底膜は、細胞外マトリックスに富み、幹細胞の維持や運命決定に必須な微小循環を提供しています。表皮の基底細胞は、上層に移行するに従い、増殖能を失い、分化を開始します。分化へと進んだ細胞は、有棘層、顆粒層、角質層を経て、皮膚の表層から剥がれ落ちます。表皮分化の最終段階で、細胞は核やミトコンドリア等の細胞小器官を失い、扁平な死んだ状態の細胞が重なり合う事で、角層バリアを形成します。この様に、古くなった細胞は垢となって脱落しますが、表皮幹細胞によって新しい細胞が常に供給されるので、組織の恒常性は保たれます。
また、皮膚には、毛包や皮脂腺、汗腺等の付属器が備わっており、夫々が固有の機能を有しています。毛周期に応じた毛の周期的な生え変わりは、皮膚のバルジ領域に存在する毛包幹細胞によって支えられます。毛包間表皮と毛包の幹細胞は、恒常状態ではお互いに独立して働いていますが、損傷やストレスに応答して、異なる系統に分化する事もあります。加齢によって、毛包幹細胞から表皮系譜への異所的分化や移動、幹細胞の枯渇が起こり、脱毛や白髪の原因になります(美容通信2022年12月号)(美容通信2027年3月号)。
皮膚は、再生能力の高い臓器の一つで、些細な傷であれば、唾を付けとくだけで勝手に治ってしまいます。この様な自己再生能の高さから、再生医療の先駆けとしては、表皮幹細を体外に取り出して培養、作成した培養表皮シートの移植が、広範囲熱傷等の治療として形成外科領域では頻用されていました。HISAKOも四半世紀前になりますが、培養表皮シートの入ったBOXを抱えて、大学病院の救命救急センターの手術室と培養センターの間を何度も往復したものです。しかし、皮膚の再生医療の多くは表皮組織の再生に限られ、多様かつ複雑な皮膚の機能や三次元構造を完全に再生する事は、未だに困難な状況です。
皮膚幹細胞の分裂不均一性
組織幹細胞は、細胞分裂頻度を抑える事で、DNA損傷や遺伝子変異、テロメア短縮(美容通信2024年9月号)等の影響を最小限にし、老化や癌を防ぐと考えられて来ました。低頻度分裂の組織幹細胞では、一般に代謝状態が低く抑えられており、特殊なニッチ環境に置かれる事で、長期的な内的・外的ストレスから保護されていますが…、しかし、その事が本当に幹細胞の老化を遅らせるメカニズムとして機能しているのかは、不明です。
毛包では、低頻度分裂細胞が長期的な幹細胞として、細胞系譜(ヒエラルキー)の頂点に位置し、活発に分裂する前駆細胞を生み出すと考えられています。毛包幹細胞は毛周期に応じて活性化されますが、これには毛周期の真皮や毛乳頭、脂肪細胞等の環境からのシグナルと、毛包幹細胞に於ける自律的因子(エピゲノム(美容通信2022年6月号)や転写因子等)が強調して働く事が重要です。マウスのお話になりますが、マウスの毛包ではバジルに位置する毛包幹細胞の分裂速度は、毛周期1回につき1~5回程度で、生涯を通じての平均分裂回数が100回以下と推定されています。毛包幹細胞が低分裂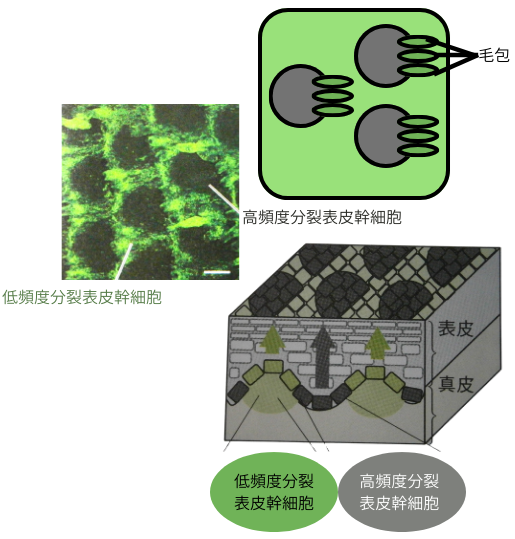 状態に保たれている事は、長期的な幹細胞機能の維持には重要と考えられています。
状態に保たれている事は、長期的な幹細胞機能の維持には重要と考えられています。
また、人ではなくてマウスの話ではありますが、毛包間表皮には低頻度分裂細胞と高頻度分裂細胞がありますが、彼らは皮膚の別々の場所に大きなクラスターを作り、規則的に局在しています。これ等は、恒常状態では独立して働きますが、大きな損傷を受けた後の損傷修復過程では、両方の幹細胞が盛んに増殖するだけでなく、互いの領域への移動が観察されるそうです。しかし興味深い事に、損傷後3ヶ月が経過して傷が癒える=戦後混乱期が終わると、2種類の表皮幹細胞とその子孫細胞達は、先祖代々の土地に夫々帰還し、平常時の生活に戻ります。異国での派兵生活は、長続きしないようです。
表皮幹細胞の下には、真皮の線維芽細胞が位置し、表皮‐真皮間のシグナルを通して、表皮幹細胞の空間的な局在を制御しています。表皮幹細胞の増殖に働くニッチシグナルの一つであるEGFRの負の制御因子Lrig1は、低頻度分裂領域に於いて生後初期に発現が開始し、表皮幹細胞の直下で不均一なパターンを形成します。古典的なWntシグナルは、高頻度分裂な表皮幹細胞に於いて活性化を示し、表皮幹細胞の分裂不均一性の制御に働いていると考えられています。
加齢に伴う皮膚幹細胞の変容
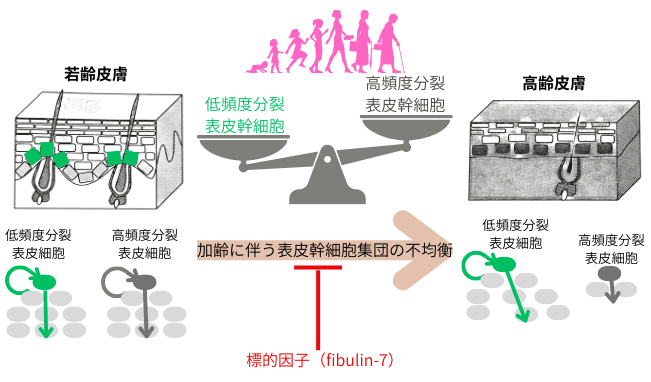 若い人の皮膚では、不均一な表皮幹細胞集団が組織の恒常性を維持しますが、加齢によってこの幹細胞集団に不均衡が生じ、高頻度分裂の幹細胞集団が喪失します。
若い人の皮膚では、不均一な表皮幹細胞集団が組織の恒常性を維持しますが、加齢によってこの幹細胞集団に不均衡が生じ、高頻度分裂の幹細胞集団が喪失します。
fibulin-7は、基底膜に局在し、加齢と共に発現が減少する事が知られています。fibulin-7を謙遜したマウスでは、分裂頻度の高い表皮幹細胞クローンの減少が促進すると共に、創傷治癒が遅延する等、皮膚老化の様相を示す事が知られています。fibulin-7は、細胞外マトリックス蛋白質との物理的な相互作用を通じて、表皮幹細胞の微小循環を維持し、幹細胞を分裂や炎症ストレスから保護する機能を有する抗老化マトリックスと考えられています。
皮膚老化と血管
老化はあらゆる臓器に於いて、機能低下を引き起こします。若い頃には、組織に多少の問題が起こっても、とっとと修復がなされてしまいますが、年を取ると、小さな綻びも積み重なって、組織の機能低下が誘導されます。皮膚も例外ではなく、加齢に伴い、皮膚の菲薄化、線維化が起き、硬化するだけでなく、毛髪の減少、色素沈着、皺、弛み等が起こって来ます。皮膚の老化の因子は多岐に亘り、紫外線によるダメージの蓄積、外的ストレス、生活習慣等が代表的なものです。
皮膚は、表皮、真皮、皮下組織の三層構造から成り立っており、血管は主に真皮層と皮下組織に分布しており、栄養供給や老廃物の排出、温度調節等の様々な機能を有しています。また、血管内皮細胞は皮膚の恒常性維持に必要な成長因子やサイトカインの分泌に寄与しており、炎症反応や創傷治癒に於いても重要な役割を果たしています。
皮膚と血管
皮膚表皮には、前述の様に、毛包と毛包間表皮が存在し、夫々に幹細胞が存在し、毛包幹細胞、毛包間表皮幹細胞が皮膚の恒常性の維持に重要です。毛包は、表皮から真皮に向かって下方に突出する皮膚付属器です。その為、真皮に存在する血管と密接な関係があります。Vasculature niche(血管系ニッチ)は、造血幹細胞、神経幹細胞、筋幹細胞等のっ組織幹細胞と相互作用が認められており、幹細胞プールの恒常性と維持に重要と考えられています。更には、幹細胞が隣接する内皮細胞を誘導し、創傷治癒を促す事も分かっています。
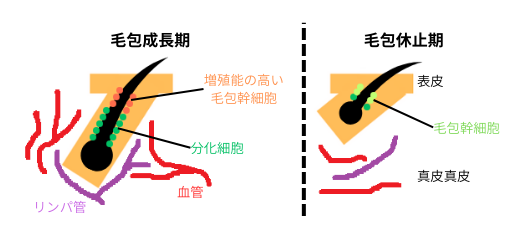 毛包には毛周期があり、成長期には毛包幹細胞が増殖と分化を繰り返す事で、毛包が伸長します。退行期には、アポトーシスにより細胞が減少し、毛包が縮小します。休止期には、細胞周期が遅くなり、静止状態となりますが、再度成長期に移行する…。常習的に、これをぐるぐる繰り返しています。左図の如く、成長期では血管新生が誘導され、それにより、酸素と栄養を基質前駆細胞に供給し、毛幹の成長を促進します。退行期では、毛包の退縮と共に、周囲の血管が破壊してしまいます。この様な血管の変化は、毛包ケラチノサイトに於けるVEGFの抑制及びTSP-1の発現上昇により起こります。成長期に毛包幹細胞が活性化すると、通常は皮下組織で水平に配置されて毛芽に集約されている血管は、一気に増殖して、真皮内の毛包、表皮に向けて垂直に盛んに伸び上がります。退行期になると、血管は元の穏やかな凪状態に戻り、毛包下にこじんまりとまとまった血管構造に戻ります。この様な、毛周期と密接に繋がる血管の構造変化には、Runx1の存在が関与していると考えられています。
毛包には毛周期があり、成長期には毛包幹細胞が増殖と分化を繰り返す事で、毛包が伸長します。退行期には、アポトーシスにより細胞が減少し、毛包が縮小します。休止期には、細胞周期が遅くなり、静止状態となりますが、再度成長期に移行する…。常習的に、これをぐるぐる繰り返しています。左図の如く、成長期では血管新生が誘導され、それにより、酸素と栄養を基質前駆細胞に供給し、毛幹の成長を促進します。退行期では、毛包の退縮と共に、周囲の血管が破壊してしまいます。この様な血管の変化は、毛包ケラチノサイトに於けるVEGFの抑制及びTSP-1の発現上昇により起こります。成長期に毛包幹細胞が活性化すると、通常は皮下組織で水平に配置されて毛芽に集約されている血管は、一気に増殖して、真皮内の毛包、表皮に向けて垂直に盛んに伸び上がります。退行期になると、血管は元の穏やかな凪状態に戻り、毛包下にこじんまりとまとまった血管構造に戻ります。この様な、毛周期と密接に繋がる血管の構造変化には、Runx1の存在が関与していると考えられています。
血管の老化
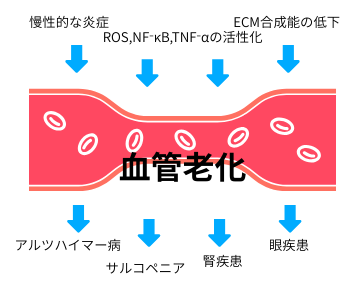 心血管系及び脳血管系の疾患は、日本に於ける高齢者の死因の上位を占めています。慢性的な炎症、ROS(美容通信2017年10月号)、NF-κB(美容通信2021年1月号)、TNF-α(美容通信2024年3月号)の活性化、ECM(美容通信2021年8月号)合成能の低下は、血管老化の一因となります。これ等の加齢によって誘発される微小循環の機能的・構造的変化は、血管性認知障害(美容通信2027年5月号)(美容通信2024年10月号)、アルツハイマー病(美容通信2019年4月号)、サルコペニア(美容通信2019年2月号)、腎疾患(美容通信2026年10月号)、眼疾患(美容通信2023年6月号)等、様々な加齢性疾患の病因に関与しています。
心血管系及び脳血管系の疾患は、日本に於ける高齢者の死因の上位を占めています。慢性的な炎症、ROS(美容通信2017年10月号)、NF-κB(美容通信2021年1月号)、TNF-α(美容通信2024年3月号)の活性化、ECM(美容通信2021年8月号)合成能の低下は、血管老化の一因となります。これ等の加齢によって誘発される微小循環の機能的・構造的変化は、血管性認知障害(美容通信2027年5月号)(美容通信2024年10月号)、アルツハイマー病(美容通信2019年4月号)、サルコペニア(美容通信2019年2月号)、腎疾患(美容通信2026年10月号)、眼疾患(美容通信2023年6月号)等、様々な加齢性疾患の病因に関与しています。
皮膚老化に於ける血管の重要性
皮膚血管系は、酸素と栄養を供給しています。老化による血管の減少は、直接的に皮膚の恒常性を低下させますが、この分野については未だ解明されていない事も多く、未だ未だ発展途上です。最近は、力学的刺激に対して細胞が如何に応答するかに着目したメカノバイオロジーと老化の関係が注目されています。
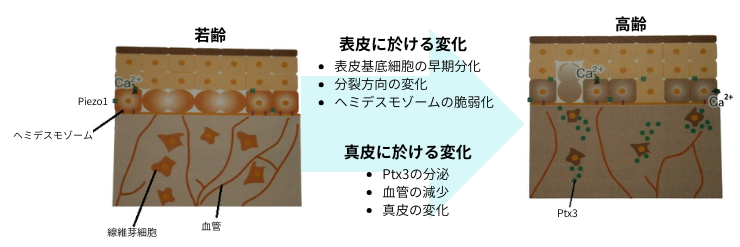
下図は、加齢に伴う力学的変化に着目した皮膚老化のメカニズムの図です。
加齢により、線維芽細胞はPtx3を分泌する様になりますが、これにより血管が減少し、真皮が硬化します。それを感知した表皮基底細胞に於いて、Piezo1を介した、過剰なCa2+の流入が起こります。これにより、表皮基底細胞の早期分化、分裂方向の変化、ヘミデスモゾームの脆弱化が起きます。
皮膚の老化とケラチノサイト
皮膚は、加齢の影響が見た目の変化として認識されやすいだけでなく、免疫系の機能低下や皮膚癌の多発傾向が高齢者に多く認められます。また、皮膚は、他の臓器と比べて環境と身体の境界線としての独自の機能も果たし、日々、様々な環境要因(紫外線、大気汚染、乾燥、アレルゲン、病原微生物等)に曝されています。中でも、皮膚の再表面に位置する表皮は、加齢や紫外線を始めとする環境要因の影響を受けやすく、機能が低下しやすい事が知られています。
加齢に伴う表皮の変化(老化)
加齢した表皮では、最表面の角層の脂質の合成能低下による減少や、pH上昇により酸性状態が損なわれたりする等々により、表皮バリアの機能の低下が起こります。これにより、薬物透過性の変化、刺激性接触皮膚炎の対する感受性の増加、しばしば乾皮症を呈しますが、皮膚局所の炎症の惹起のみならず、全身の炎症状態に繋がります。
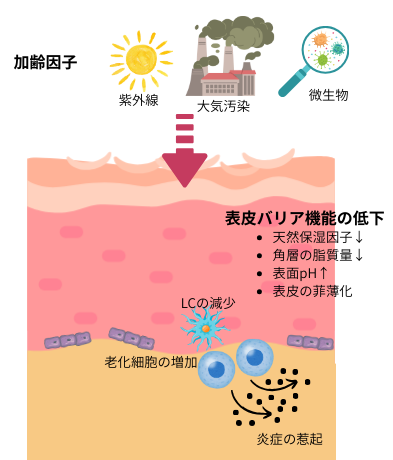 また、加齢に伴って生体内に蓄積する老化細胞が、慢性炎症を惹起した挙句に、組織や臓器の機能低下を齎し、老化や加齢関連疾患病態に関与しています。表皮に於いても、老化細胞の蓄積と同時に、菲薄化を伴う表皮の老化が認められ、ケラチノサイトを含む表皮細胞の老化が表皮機能の破綻を誘導していると考えられています。
また、加齢に伴って生体内に蓄積する老化細胞が、慢性炎症を惹起した挙句に、組織や臓器の機能低下を齎し、老化や加齢関連疾患病態に関与しています。表皮に於いても、老化細胞の蓄積と同時に、菲薄化を伴う表皮の老化が認められ、ケラチノサイトを含む表皮細胞の老化が表皮機能の破綻を誘導していると考えられています。
左図を見て下さい。表皮には、ランゲルハンス細胞やメラノサイト等の免疫や色素形成に係る細胞も存在しますが、加齢によりそれらの細胞も質的・量的変化を起こし、皮膚の恒常性の破綻に繋がります。マクロファージの一種であるランゲルハンス細胞は、環境と身体の境界線上で、外敵に対する見張り役の免疫細胞として目を光らせています。しかし、加齢に伴い退役する細胞が増えると、当然ながら、皮膚の免疫戦線は弱体化します。更には、メラニン色素を供給するメラノサイトも老い曝えて、婆の佃煮状態と揶揄される如くに表皮に蓄積し、それが周囲のケラチノサイトにも悪影響を及ぼして、表皮の老化を進行させてしまいます。
皮膚老化とケラチノサイト
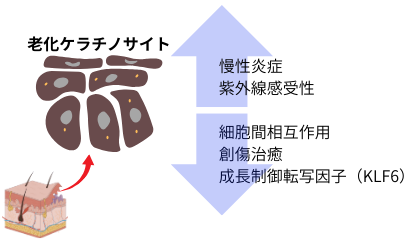 表皮の層別解析及び細胞間の相互解析により、基底層と有棘層の増殖ケラチノサイトが、加齢により細胞間のコミュニケーションが減少しているだけでなく、紫外線に対する感受性亢進、転写因子KLF6の発現低下やp63等の転写因子のクロマチン領域等の変化が観察され、表皮の老化に関与していると考えられています。
表皮の層別解析及び細胞間の相互解析により、基底層と有棘層の増殖ケラチノサイトが、加齢により細胞間のコミュニケーションが減少しているだけでなく、紫外線に対する感受性亢進、転写因子KLF6の発現低下やp63等の転写因子のクロマチン領域等の変化が観察され、表皮の老化に関与していると考えられています。
関連ページ
関連するHISAKOの美容通信をピックアップしました。
来月号の予告
NMNの基礎から臨床まで~加齢性変化に対する臨床効果の可能性~
<NMN補充>