HISAKOの美容通信2026年10月号
加齢と腎臓に於けるオートファジーの働き&最新のトピックス・細胞老化に対する老化ワクチン
 性差にも関連しますが、性ホルモンもオートファジー制御に重要な要因です。アンドロゲン受容体ARもオートファジーと関連しており、腎臓だけでなく、様々な臓器障害の性差に関係があるのかも知れません。慢性腎臓病は男性に多く、急性腎障害から慢性に移行し易い事が知られています。加齢に伴って、オートファジーの機能が非常に高まった状態が長く続いていると、オートファジーの機能自体が疲労してしまうと言うか…だんだんと擦り減って、ストレスに対する応答性が低下します。それによってミトコンドリアの異常、DNAの異常、様々な凝集蛋白が尿細管細胞に蓄積し、腎臓の老化が亢進します。つまり、慢性腎臓病は、全身の老化を促進して、例えばフレイルであったり、心臓病を促進してしまいます。オートファジーの機能を制御する事によって、これ等の治療の可能性が指摘されています。
性差にも関連しますが、性ホルモンもオートファジー制御に重要な要因です。アンドロゲン受容体ARもオートファジーと関連しており、腎臓だけでなく、様々な臓器障害の性差に関係があるのかも知れません。慢性腎臓病は男性に多く、急性腎障害から慢性に移行し易い事が知られています。加齢に伴って、オートファジーの機能が非常に高まった状態が長く続いていると、オートファジーの機能自体が疲労してしまうと言うか…だんだんと擦り減って、ストレスに対する応答性が低下します。それによってミトコンドリアの異常、DNAの異常、様々な凝集蛋白が尿細管細胞に蓄積し、腎臓の老化が亢進します。つまり、慢性腎臓病は、全身の老化を促進して、例えばフレイルであったり、心臓病を促進してしまいます。オートファジーの機能を制御する事によって、これ等の治療の可能性が指摘されています。
右図は、Wikipediaから拝借した写真ですが、ロンドンでベルギーからの移民の子として生まれたクリスチャン・ルネ・ド・デューブは、国際的に高く評価された細胞生物学者で生化学者です。1963年に細胞が自身のタンパク質を小胞としてリソソームと融合して分解する現象をオートファジー、その小胞をオートファゴソームと命名しました。1974年には、細胞小器官の構造と機能に関する発見で、アルベルト・クラウデ、ジョージ・エミール・パラーデとともにノーベル生理学・医学賞を受賞しました。まあ、オートファジーの父です。
先日行われた第16回泌尿器抗加齢医学研究会から、面白そうな内容をピックアップしてみました。併せて、最近よく耳にする「老化ワクチン」について解説しています。
加齢と腎臓に於けるオートファジーの働き
慢性腎臓病にも、性差がある。
 国民の8人に一人は慢性腎臓病(CKD)患者と言われています。透析導入患者は元々男性が多いですが、その男女差は年々大きくなる傾向があります。
国民の8人に一人は慢性腎臓病(CKD)患者と言われています。透析導入患者は元々男性が多いですが、その男女差は年々大きくなる傾向があります。
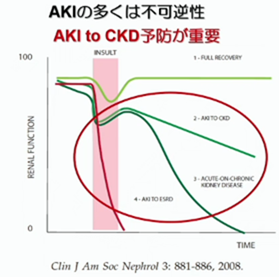
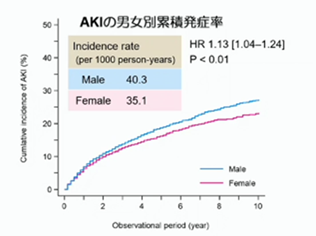 急性腎障害(AKI)の多くは実は不可逆性で、急性腎障害から慢性腎臓病への移行が問題になっています。実は、急性腎障害の頻度にも左図の様に性差があり、女性よりも男性に起こりやすい事が知られています。
急性腎障害(AKI)の多くは実は不可逆性で、急性腎障害から慢性腎臓病への移行が問題になっています。実は、急性腎障害の頻度にも左図の様に性差があり、女性よりも男性に起こりやすい事が知られています。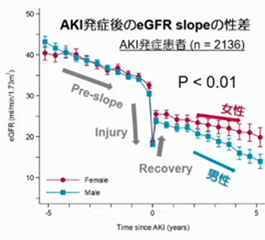 ここで、注目してもらいたいのは、急性腎障害を起こすと、eGFRはある程度は一旦は回復しますが、ここに大きな性差があり、女性はその後ほぼ同じ位のスピードで緩やかにeGFRは低下するのですが、男性はより急峻に一気に奈落の底に向かって転げ落ちます。
ここで、注目してもらいたいのは、急性腎障害を起こすと、eGFRはある程度は一旦は回復しますが、ここに大きな性差があり、女性はその後ほぼ同じ位のスピードで緩やかにeGFRは低下するのですが、男性はより急峻に一気に奈落の底に向かって転げ落ちます。
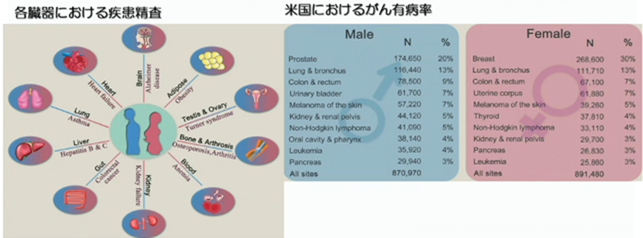
左図の如くに、様々な疾患で男女差がある事は良く知られています。精巣や子宮以外にも、前述の通り、腎臓についても男性では腎不全が起こりやすいですし、腎泌尿器系の癌についても、男性は多くなっています。
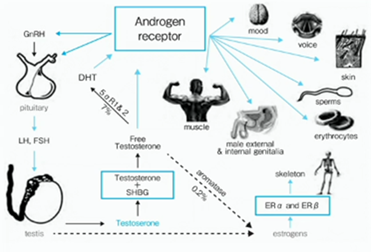 右図は、男性に於けるアンドロゲン産生と作用を示した図です。
右図は、男性に於けるアンドロゲン産生と作用を示した図です。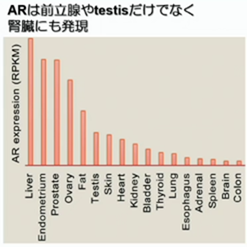 アンドロゲン受容体は、腎臓にも発現しており、もしかしたら、それが様々な臓器障害の性差に関係があるのかも知れません(美容通信2025年10月号)(美容通信2026年2月号)。因みに宣伝ですが、来月号の美容通信は、性差医学にスポットを当てた特集です。
アンドロゲン受容体は、腎臓にも発現しており、もしかしたら、それが様々な臓器障害の性差に関係があるのかも知れません(美容通信2025年10月号)(美容通信2026年2月号)。因みに宣伝ですが、来月号の美容通信は、性差医学にスポットを当てた特集です。
腎障害の進展のメカニズム
病態メカニズムの解明は腎臓に限らずとても重要で、これに基づいて治療方法を開発する必要があります。
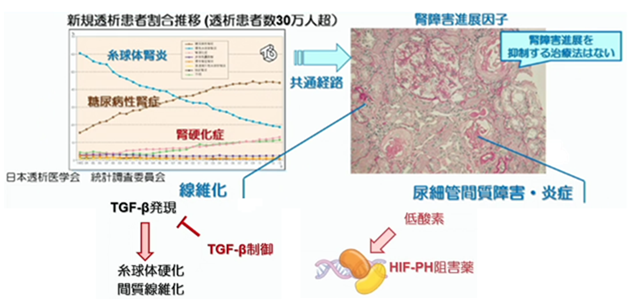 糸球体腎炎、糖尿病性腎症、腎硬化症は、原因が異なる全く別の疾患ではありますが、ある程度症状が進展すると、共通経路で、腎障害の進展因子として働き、腎臓は坂を転げ落ちるかのようにどんどん悪くなります。しかしながら、現状では、腎障害進展を抑制する十分な方法は確立していません。例えば、線維化に対してはTGF-ベータが関与しています。ですから、このTGF-βを制御さえすれば、糸球体硬化や間質線維化が抑制されるはずなんですが…、未だ、成果は上がっていません。また、腎障害に於ける腎の低酸素が腎障害に於ける進展因子と言う説もあります。しかし、低酸素を阻害するHIF-PH阻害薬が腎臓病の進展するかと言うと…、そう言ったエビデンスは得られませんでした。
糸球体腎炎、糖尿病性腎症、腎硬化症は、原因が異なる全く別の疾患ではありますが、ある程度症状が進展すると、共通経路で、腎障害の進展因子として働き、腎臓は坂を転げ落ちるかのようにどんどん悪くなります。しかしながら、現状では、腎障害進展を抑制する十分な方法は確立していません。例えば、線維化に対してはTGF-ベータが関与しています。ですから、このTGF-βを制御さえすれば、糸球体硬化や間質線維化が抑制されるはずなんですが…、未だ、成果は上がっていません。また、腎障害に於ける腎の低酸素が腎障害に於ける進展因子と言う説もあります。しかし、低酸素を阻害するHIF-PH阻害薬が腎臓病の進展するかと言うと…、そう言ったエビデンスは得られませんでした。
腎臓の老化
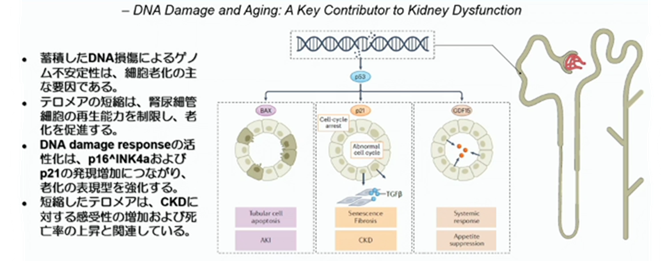
抗老化と言う点で考えると、老化に伴ってDNAの損傷が生じます。蓄積したDNAの損傷は、ゲノムの不安定性を生じ、これが細胞老化の主要な要因となります。また、テロメアの短縮(美容通信2024年9月号)(美容通信2022年7月号)自体が、腎臓の老化、腎臓の尿細管細胞の再生を制限し、老化を促進させます。DNAが障害される為に、p16INK4a、p21の発現が増加し、老化の表現型が強化されます。短縮したテロメアは、慢性腎臓病に対する感受性の増加及び死亡の上昇と関連します。DNAの障害によりp53の発現が増加しますが、BAXの尿細管での発現を介して、アポトーシスや急性腎障害を生じさせます。また、P21は細胞周期に関連しており、線維化や慢性腎臓病と関係があります。GDF15は脳等から発現して、食欲を抑制すると言われていますが、腎臓の尿細管でも発現していて、これが食欲の低下、サルコペニア、フレイルと結びつくと考えられています。
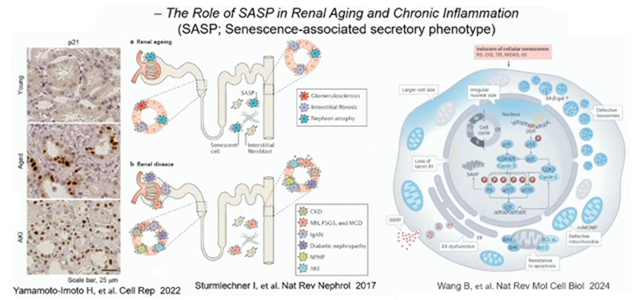
何故、老化が良くないのでしょうか? 老化細胞自体がSASPを発現する事で、炎症を惹起します。Inflammation(炎症)とaging(加齢/老化)を併せたInflammaging(インフラメイジング)なる造語も出現していますが、様々なエイジング、腎疾患に関連して尿細管細胞で老化細胞が発現し、これがSASPを発現、炎症を惹起するとされています。
糸球体でも老化細胞が出現するとはされていますが、尿細管特異的にp21が発現します。若年では確認出来ませんが、加齢の腎生検スライドでは、尿細管細胞にp21が発現しているのが分かります。上の図は移植腎のドナーの腎生検ですが、急性腎障害と言われる部位にはp21が発現しているのが分かります。老化に伴って、様々なリソソームやミトコンドリア、小胞と言ったオルガネラでの障害が起こり、SASPが生じます。
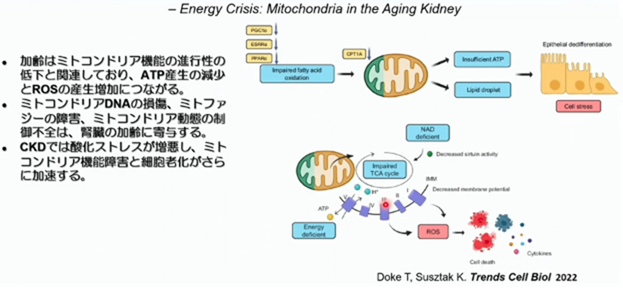 また、加齢は、ミトコンドリア(美容通信2017年7月号)(美容通信2022年7月号)の機能障害と関連しており、ATPの産生の減少や活性酸素の増加にも繋がっています。ミトコンドリアDNAの損傷、ミトファジーの障害、ミトコンドリア動態の機能不全は、腎臓に於ける加齢に寄与しています。慢性腎臓病では酸化ストレスが増悪し、ミトコンドリアの機能障害と細胞老化が更に加速します。
また、加齢は、ミトコンドリア(美容通信2017年7月号)(美容通信2022年7月号)の機能障害と関連しており、ATPの産生の減少や活性酸素の増加にも繋がっています。ミトコンドリアDNAの損傷、ミトファジーの障害、ミトコンドリア動態の機能不全は、腎臓に於ける加齢に寄与しています。慢性腎臓病では酸化ストレスが増悪し、ミトコンドリアの機能障害と細胞老化が更に加速します。
Cellって雑誌をご存じでしょうか? Cellはアメリカのセル出版が発行している、1974年創刊の隔週刊の科学学術雑誌で、医学・生化学・分子生物学等、ライフサイエンス分野に於ける世界最高峰の学術雑誌です。嗅覚受容体の発見、テロメアの機能の解明、iPS細胞の開発をはじめとするノーベル生理学・医学賞の対象となった論文等、医学史・科学史に残る論文が多い事でも有名です。 しかし、2007年9月7日付の表紙に、「ジョジョの奇妙な冒険」等で知られる漫画家・荒木飛呂彦のイラスト(同誌に掲載された瀬藤光利・自然科学研究機構生理学研究所准教授らの依頼で研究内容をイメージ化したもの)を採用した事で、HISAKOの様な通常の読者層とは違う方面からも注目を浴びました。日本の漫画が著名な学術誌の表紙を飾る。…実に、インパクト抜群な大事件でした。折角ですから、脱線ついでにちょっとばかり解説加えますと、SCRAPPERは、アクティブ・ゾーンのタンパク質RIM1にユビキチンを付加し、分解へと導きます。 この図では、人型のものをSCRAPPER、円盤形のものをRIM1、小さいハート型のものをユビキチンとして表し、SCRAPPERがRIM1にユビキチンを付加していく様子を擬人化して表現しているんだそうです。
しかし、2007年9月7日付の表紙に、「ジョジョの奇妙な冒険」等で知られる漫画家・荒木飛呂彦のイラスト(同誌に掲載された瀬藤光利・自然科学研究機構生理学研究所准教授らの依頼で研究内容をイメージ化したもの)を採用した事で、HISAKOの様な通常の読者層とは違う方面からも注目を浴びました。日本の漫画が著名な学術誌の表紙を飾る。…実に、インパクト抜群な大事件でした。折角ですから、脱線ついでにちょっとばかり解説加えますと、SCRAPPERは、アクティブ・ゾーンのタンパク質RIM1にユビキチンを付加し、分解へと導きます。 この図では、人型のものをSCRAPPER、円盤形のものをRIM1、小さいハート型のものをユビキチンとして表し、SCRAPPERがRIM1にユビキチンを付加していく様子を擬人化して表現しているんだそうです。
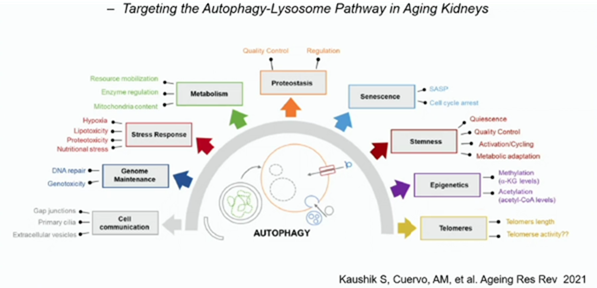
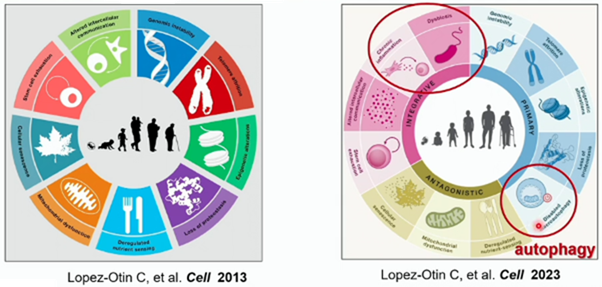 2013年と2023年のCellに、老化を規定する因子が報告されていますが、2023年のCellでは9因子から12因子に増加しました。増えたのがオートファジーとDysbiosisと慢性炎症(美容通信2021年1月号)の3つの項目です。Dysbiosis(美容通信2020年6月号)(美容通信2024年8月号)とは、腸内細菌叢の異常状態で、炎症性腸疾患やメタボリック症候群等の疾患と関連する事が分かっています。オートファジー(美容通信2026年2月号)(美容通信2024年1月号)は、genomeの安定性や、proteostasis、mitochondriaの障害に関係しています。
2013年と2023年のCellに、老化を規定する因子が報告されていますが、2023年のCellでは9因子から12因子に増加しました。増えたのがオートファジーとDysbiosisと慢性炎症(美容通信2021年1月号)の3つの項目です。Dysbiosis(美容通信2020年6月号)(美容通信2024年8月号)とは、腸内細菌叢の異常状態で、炎症性腸疾患やメタボリック症候群等の疾患と関連する事が分かっています。オートファジー(美容通信2026年2月号)(美容通信2024年1月号)は、genomeの安定性や、proteostasis、mitochondriaの障害に関係しています。
オートファジー
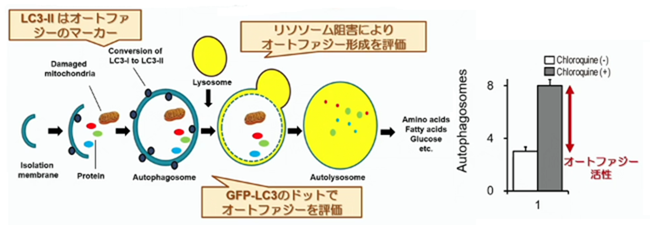 オートファジーは、真核生物に普遍的に保たれている細胞内の主要な分解機構です。飢餓状態になると、エネルギーの供給源として、オルガネラ等を分解する事で、アミノ酸や脂質等の産生に関わります。LC3-Ⅱはオートファジーのマーカーで、このLC3-ⅡをGFP-LC3のドットでマークしたものが、オートファジーのマーカーとして使用されます。リソソームの障害によって、オートファジーの形成を評価しますが、例えば、リソソームの働きを止めるクロロキンで止めて、生じた差をオートファジーの活性として評価します。
オートファジーは、真核生物に普遍的に保たれている細胞内の主要な分解機構です。飢餓状態になると、エネルギーの供給源として、オルガネラ等を分解する事で、アミノ酸や脂質等の産生に関わります。LC3-Ⅱはオートファジーのマーカーで、このLC3-ⅡをGFP-LC3のドットでマークしたものが、オートファジーのマーカーとして使用されます。リソソームの障害によって、オートファジーの形成を評価しますが、例えば、リソソームの働きを止めるクロロキンで止めて、生じた差をオートファジーの活性として評価します。
 ミトコンドリアDNAは2本鎖の円形DNAで、酸化的リン酸化の酵素等をコードしています。99の臨床表現型を持つ約15万人の日本人を対象に、phenome(網羅的表現型情報)であるwide association studyを行いました。CreatinineやeGFRと関連しているのが、co1。ミトコンドリアの酸化的リン酸化に関する酵素が、腎機能と関連しています。
ミトコンドリアDNAは2本鎖の円形DNAで、酸化的リン酸化の酵素等をコードしています。99の臨床表現型を持つ約15万人の日本人を対象に、phenome(網羅的表現型情報)であるwide association studyを行いました。CreatinineやeGFRと関連しているのが、co1。ミトコンドリアの酸化的リン酸化に関する酵素が、腎機能と関連しています。
尿細管細胞は様々なものを再吸収する為、エネルギーを大量に消費します。ですから、尿細管細胞はミトコンドリアが豊富な細胞です。通常状態で、オートファジーがきちんと機能していれば、ミトコンドリアが酸化ストレスや蛋白等が障害されるような事態に遭遇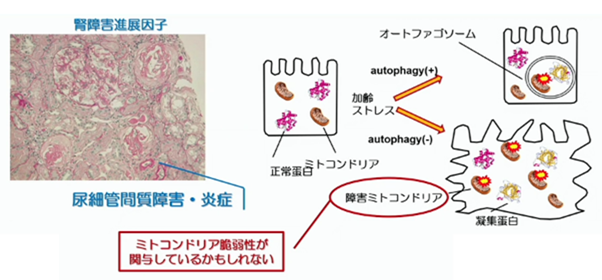 しても、オートファジーがそれらをきちんと処理?消去?してくれます。しかしオートファジーの働きが滞ると、尿細管細胞に障害されたミトコンドリアや蛋白等が蓄積してしまい、ゴミ屋敷状態に! これが細胞障害に繋がります。
しても、オートファジーがそれらをきちんと処理?消去?してくれます。しかしオートファジーの働きが滞ると、尿細管細胞に障害されたミトコンドリアや蛋白等が蓄積してしまい、ゴミ屋敷状態に! これが細胞障害に繋がります。
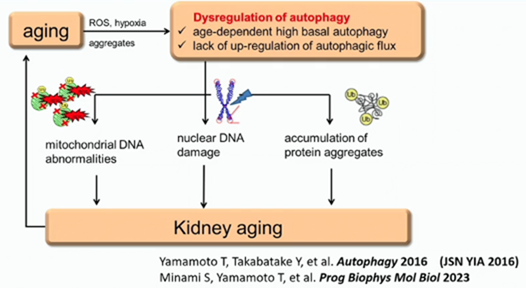 ですから、ミトコンドリアの脆弱性が腎障害と関連しているのかも知れません。加齢も関連しているかも知れません。そもそも加齢に伴って、オートファジーの機能が非常に高まった状態が長く続いていると、オートファジーの機能自体が疲労してしまうと言うか…だんだんと擦り減って、ストレスに対する応答性が低下します。それによってミトコンドリアの異常、DNAの異常、様々な凝集蛋白が尿細管細胞に蓄積し、腎臓の老化が亢進します。
ですから、ミトコンドリアの脆弱性が腎障害と関連しているのかも知れません。加齢も関連しているかも知れません。そもそも加齢に伴って、オートファジーの機能が非常に高まった状態が長く続いていると、オートファジーの機能自体が疲労してしまうと言うか…だんだんと擦り減って、ストレスに対する応答性が低下します。それによってミトコンドリアの異常、DNAの異常、様々な凝集蛋白が尿細管細胞に蓄積し、腎臓の老化が亢進します。
加齢とオートファジー
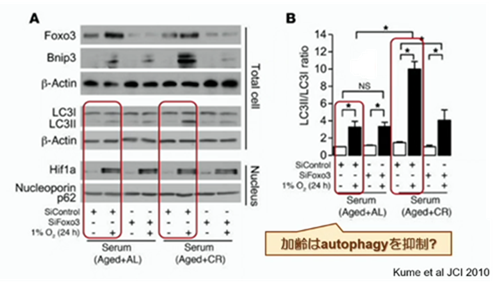 右の図を見て下さい。カロリー制限をしていると、老化が抑制されます。カロリー制限していると、オートファジーの機能が亢進します。しかし、抗老化因子のSiFoxo3をノックダウンすると、オートファジーの機能が抑制されます。つまり、どうやら、加齢はオートファジーを抑制するのではないかと推測されます。
右の図を見て下さい。カロリー制限をしていると、老化が抑制されます。カロリー制限していると、オートファジーの機能が亢進します。しかし、抗老化因子のSiFoxo3をノックダウンすると、オートファジーの機能が抑制されます。つまり、どうやら、加齢はオートファジーを抑制するのではないかと推測されます。
![]() Rubiconはオートファジーを抑制します。ですから、Rubicon KOマウスでは、オートファジーが亢進するので、結果、寿命が延長します。しかし、オートファジーに必須のAtg18も同時にノックダウンしてみると、折角の伸びた長寿命効果は相殺されてしまいました。
Rubiconはオートファジーを抑制します。ですから、Rubicon KOマウスでは、オートファジーが亢進するので、結果、寿命が延長します。しかし、オートファジーに必須のAtg18も同時にノックダウンしてみると、折角の伸びた長寿命効果は相殺されてしまいました。
オートファジーの成熟に於いて、UVRAGやRubicon1は、リソソームとオートファジーの融合等の促進に働きます。そこにRubiconが結合すると、オートファジーとリソソームの融合が抑制されてしまいます。実際、加齢マウスに於いて、Rubiconの発現は亢進しています。Rubiconの遺伝子をノックアウトすると、腎臓の線維化も抑制されされる事が分かっています。
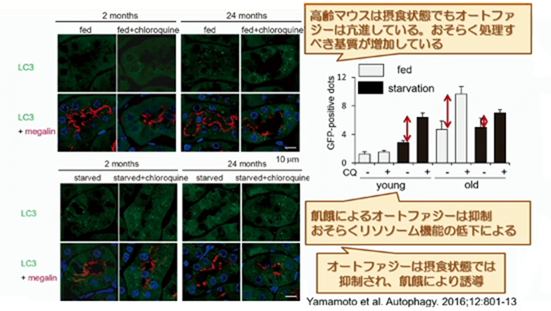 ここで、GFP-LC3 TGによるオートファジー評価をした実験についてお話します。
ここで、GFP-LC3 TGによるオートファジー評価をした実験についてお話します。
オートファジーは、飢餓状態で発現が亢進します。通常の食事をしている状態では、オートファジーは認められません。
しかし高齢マウスでは、加齢に伴って処理すべき基質が増加している為か、オートファジーは常に亢進した状態にあります。しかし問題となるのは、この様にオートファジーのレベルが常に亢進した状態が続いていると、非常事態が発生した時に、つまり、何らかのストレスが新たに掛かっても、更にオートファジーを亢進させて対応すると言う事が出来なくなってしまいます。恐らくはリソソームの機の低下が関係しているとは推測出来ますが、高齢マウスでは、飢餓状態にあっても、オートファジーが亢進しないと言うか…亢進出来ません。
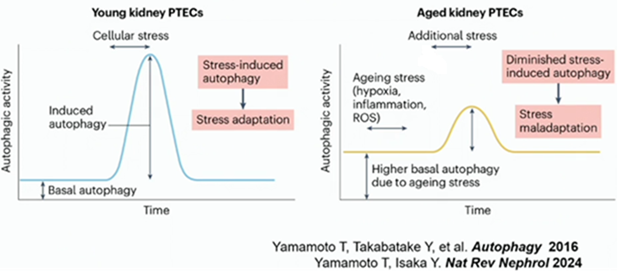 まとめると、若い時には、基底レベルのオートファジーはそれ程は高くありません。しかし、何らかのストレスが掛かっても、オートファジーが活性化して対応が出来ますから、細胞は守られます。しかし、加齢に伴って基底レベルのオートファジーが常に亢進している状態では、ストレスに対する応答性が低下しており、これが細胞障害に繋がります。
まとめると、若い時には、基底レベルのオートファジーはそれ程は高くありません。しかし、何らかのストレスが掛かっても、オートファジーが活性化して対応が出来ますから、細胞は守られます。しかし、加齢に伴って基底レベルのオートファジーが常に亢進している状態では、ストレスに対する応答性が低下しており、これが細胞障害に繋がります。
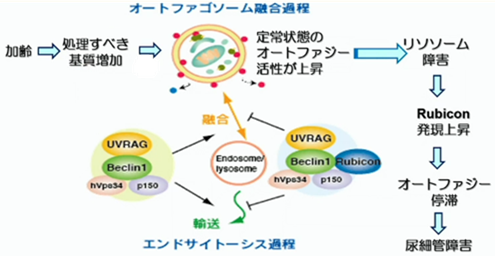 この様に処理すべき基質が増加すると、定常状態のオートファジーが常に増加していて、その下流であるリソソームが障害されます。これに伴ってRubiconの発現が上昇して、オートファジーが停滞。挙句に、何らかの偶発的事象って名前のストレスに対応する事が出来なくなって、尿細管障害に至る…。
この様に処理すべき基質が増加すると、定常状態のオートファジーが常に増加していて、その下流であるリソソームが障害されます。これに伴ってRubiconの発現が上昇して、オートファジーが停滞。挙句に、何らかの偶発的事象って名前のストレスに対応する事が出来なくなって、尿細管障害に至る…。
MondoAの役割
下の図を見て下さい。
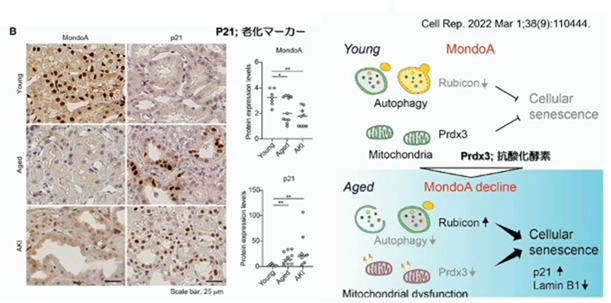
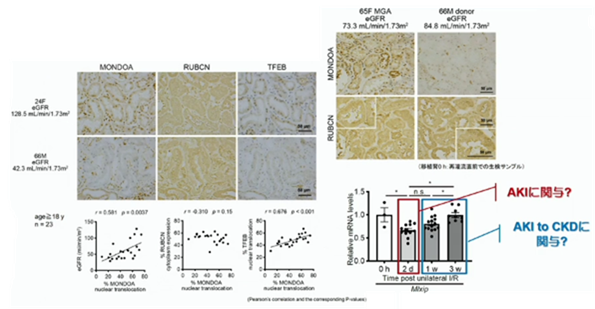
老化のマーカーであるp21が、高齢の人の尿細管細胞で亢進しています。0時間の移植腎でも、p21が亢進していますね。これと共存関係にあるのがMondoAです。時代劇『必殺シリーズ』の、中村主水とは全くの無関係です。MondoAは、若い時には尿細管細胞に発現しているのですが、高齢になると発現が低下します。0時間の移植腎に於いても、発現が低下しています。
若い時はMondoAが発現する事で、オートファジーの発現を抑制するRubiconの発現を抑制しています。或いは、抗酸化酵素であるミトコンドリアのPrdx3を発現させる事で、老化を抑制しています。しかし、高齢によってMondoAが低下して来ると、Rubiconの発現が上昇する、或いはミトコンドリアの機能が低下する事で、老化が亢進してしまいます。
実際、腎生検で若い人と高齢者を比較してみると、高齢になるとMondoAの発現が低下し、Rubiconが逆に増えています。リソソームのマスターレギュレーターであるTFEBも低下します。移植腎では、MondoAが低下する為に、Rubiconの発現が亢進して来ます。
マウスモデルに急性腎腎障害を惹起させると、虚血再開直後はMondoAの発現は低下します。これが急性腎障害の発症に関与しているのではないかと考えられています。その後、MondoAの発現は回復するのですが、これ等が上手く発現しないと、急性腎障害(AKI)から慢性腎臓病(CKD)に進行してしまうようです。
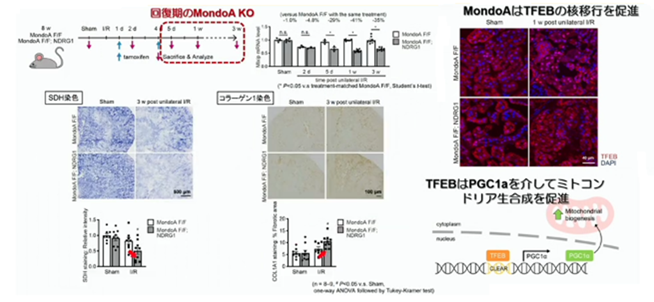
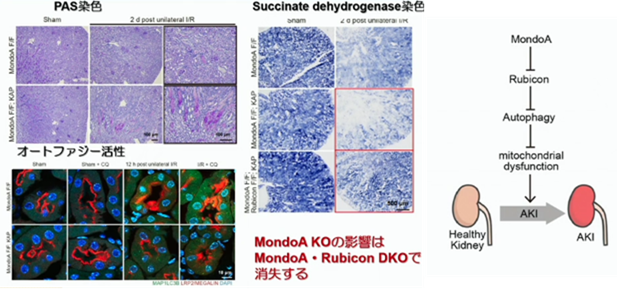 実際MondoAのノックアウトを行うと、オートファジーの活性が低下しているので、急性腎障害が増悪します。上図を見て下さい。Succinate dehydrogenase染色でミトコンドリアの機能を確認すると、MondoAのノックアウトマウスでは、ミトコンドリアの機能が非常に低下しているのが分かります。しかし、Rubiconも同時にノックアウトすると、ミトコンドリアの機能の低下は抑制されます。
実際MondoAのノックアウトを行うと、オートファジーの活性が低下しているので、急性腎障害が増悪します。上図を見て下さい。Succinate dehydrogenase染色でミトコンドリアの機能を確認すると、MondoAのノックアウトマウスでは、ミトコンドリアの機能が非常に低下しているのが分かります。しかし、Rubiconも同時にノックアウトすると、ミトコンドリアの機能の低下は抑制されます。
まとめですが、MondoAはRubiconを抑制します。Rubicon自体はオートファジーを抑制しているので、急性腎障害でMondoAが低下すると、結果的に、急性腎障害の表現型は増強されてしまいます。
急性腎障害では、最初はMondoAが低下しますが、後々回復します。下図を見て下さい。Tamoxifenで誘導されるMondoAのノックアウトを用いて、回復期のMondoAの発現を抑制してみました。白いバーでみられるMondoAは、虚血再灌流が回復すると、回復してくるものですが、回復期のMondoAの発現を抑制した状態で比べてみると、ミトコンドリアの機能が虚血再灌流の3週間後も低下したまま。コラーゲンの発現も上昇していません。線維化が起こっています。
また、MondoAは、リソソームのマスターレギュレーターであるTFEBの核移行を促進する事は知られていますが、TFEBはPGC1αを介して、ミトコンドリアの生合成を促進します。腎障害からの尿細管細胞の回復に寄与していると推測されています。
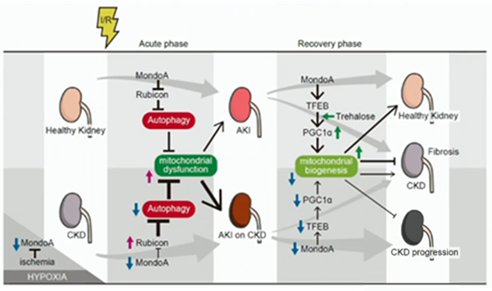 つまり、健常者、若い人はMondoAが発現しているので、Rubiconを抑制する事によって、オートファジーがきちっと働きます。しかし、高齢者ではMondoAが低下する事によって、Rubiconの発現が上昇するので、オートファジーが抑制されてしまいます。その為、急性腎障害が起こりやすくなります。回復期に関しても、TFEBを介してPGC1αが上昇する事で、ミトコンドリアの生合成が促進され、腎臓が回復するものですが、ところが高齢者ではこれが上手く行かない…。
つまり、健常者、若い人はMondoAが発現しているので、Rubiconを抑制する事によって、オートファジーがきちっと働きます。しかし、高齢者ではMondoAが低下する事によって、Rubiconの発現が上昇するので、オートファジーが抑制されてしまいます。その為、急性腎障害が起こりやすくなります。回復期に関しても、TFEBを介してPGC1αが上昇する事で、ミトコンドリアの生合成が促進され、腎臓が回復するものですが、ところが高齢者ではこれが上手く行かない…。
マスター転写因子TFEB
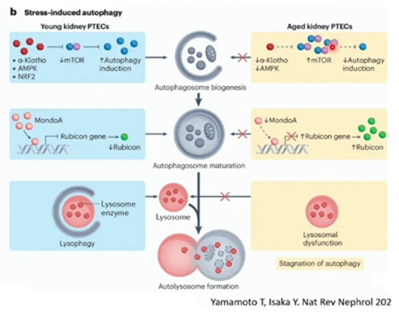 AMPKやmTORなどを介してオートファジーが出来るところ、或いは、更にはオートファジーの成熟と言うところにRubiconが関与してます。
AMPKやmTORなどを介してオートファジーが出来るところ、或いは、更にはオートファジーの成熟と言うところにRubiconが関与してます。
リソソームに関しても、高齢者と若年者では、若干異なっています。
■HKDC1
リソソームの機能を制御するマスター転写因子TFEB(Transcription Factor EB)は、ミトコンドリアの機能制御にも関わっています。TFEBが、ミトコンドリア及びリソソームにストレスを受けた際に、ヘキソキナーゼファミリーの一つであるHKDC1 (hexokinase domain containing 1)の発現を直接制御する事により、両者のクオリティーコントロールに必須の働きを持つ事が分かっています。HKDC1は、傷付いたミトコンドリアに対し、オートファジーによる除去(マイトファジー)と同時に、傷ついたリソソームの修復を促進して、細胞を健康に保ち、細胞老化を抑制します。それ故に、今後、TFEB-HKDC1経路の調節を介した老化抑制や加齢性疾患の治療法への応用が期待されているホットな研究分野です。
下図を見て下さい。
エネルギー産生を担う細胞内小器官であるミトコンドリアと、生体分子の分解を担うリソソームの機能を維持する事は、細胞を健康に保つ上で非常に重要です。又、ミトコンドリアとリソソームは、細胞内に於いて接触部位を持ってクロストークを行っており、互いの機能維持に夫々の存在が重要。つまり、嘗ての赤プリ5人組も真っ青の、持ちつ持たれつ、べったりの構造的癒着をしています。近年になって、細胞老化や様々な加齢関連疾患に於いて、損傷を受けて機能低下したミトコンドリアやリソソームが共に蓄積している事が報告され、これが細胞老化や様々な加齢関連疾患に於ける共通した特徴である事が分かって来ました。しかし、ミトコンドリア、リソソームを制御する共通の機構があるのかどうか、両者のクロストークの分子機構、またその老化における意義は不明でした。
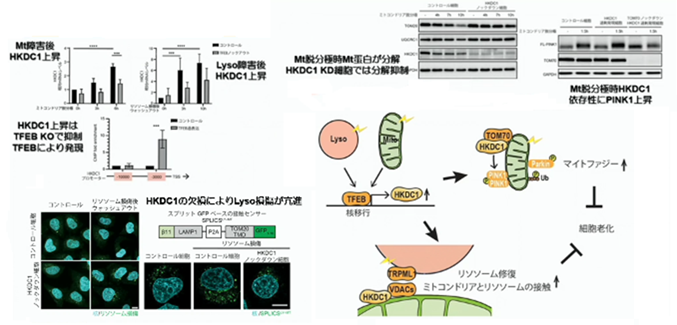
TFEBのノックアウトは、上図ではグレーのバーで示しています。ミトコンドリアが障害される、或いは、リソソームが障害されると、hexokinase domain containing1が上昇しますが、TFEBをノックダウンしておくと、その様な発現は抑制されます。チップアッセイを用いると、HKDC1の上流のところに、つまりプロモーター領域にこのTFEBが結合しているのが分かります。 ミトコンドリア障害等のミトコンドリア脱分極の時には、TOM20等の発現を介して、この分解がどんどん促進されるのですが、HKDC1がノックダウンされていると、これ等の蛋白の分解が滞ります。ミトコンドリアの分極が起ったり、ミトコンドリアの障害の時には、TOMS70等を介して、PINK1が上昇する事によって、マイトファジーは亢進します。更に、HKDC1が欠損すると、リソソームの損傷が亢進してしまいます。
*マイトファジー:老化し機能不全になったミトコンドリアを選択的に分解、排除するシステムであり、オートファジーの一種です。ミトコンドリアに対して選択的に起こる事から、”マイトファジー”と名付けられました。ミトコンドリアの脱分極や酸化ストレス、低酸素状態等の引き金に対応した、ミトコンドリアに局在する複数のカーゴ受容体が関与します。
ざっくり纏めますが、HKDC1は、ミトコンドリア損傷時に於いて、代表的な損傷ミトコンドリア除去機構であるPINK1/Parkin依存性マイトファジーを介して、損傷ミトコンドリアの除去を担います。又、リソソーム損傷時に於いては、ミトコンドリア・リソソーム接触部位を増加させ、リソソームの膜修復を促進しています。
更には、HKDC1をノックダウンした細胞では、機能低下したミトコンドリアや損傷リソソームの蓄積を伴い、細胞老化が進行します。つまり、ヘキソキナーゼファミリーの一つであるHKDC1は、解糖系の酵素として働く事が知られていますが、この機能とは独立して、ミトコンドリアとリソソームが損傷を受けた際に、TFEBはこのHKDC1を介して、これ等の損傷を修復し、老化を制御します。今後TFEB-HKDC1経路の調節を介した、老化抑制や加齢性疾患の治療法への応用が期待されています。
■パルミチン酸
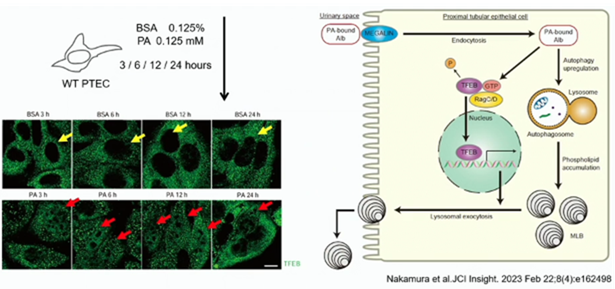
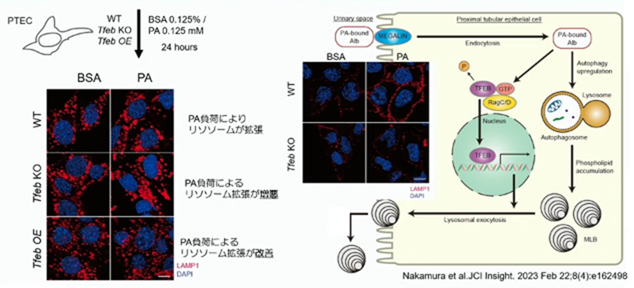
パルミチン酸は飽和脂肪酸ですが、飽和脂肪酸を投与すると、尿細管のオートファジー機能が低下して、尿細管障害或いは線維化します。パルミチン酸は、アルブミンと結合して、糸球体で濾過されて、尿細管で再吸収されますが、この際、細胞内でオートファジーを抑制します。RagC/Dの不活性化を介して、TFEBの核内移行を促進します。
ところがこのパルミチン酸は、投与すると、リソソームが拡張します。パルミチン酸負荷により、オートファジーが上手く働かないので、その下流でリソソームが蓄積して、リソソームが拡張します。TFEBをノックアウトすると、リソソームの拡張が増悪しますが、TFEBを過剰発現していると、リソソームの拡張が改善します。何故この様な事が起こって来るのかと言うと、下図を見て下さい。
TFEBをノックアウトしていないワイドタイプの場合は、細胞の周囲のところにLAMP1陽性のリソソームが認められます。ノックアウトしていると認められません。つまり、TFEBを介して、溜まったリソソームをエクソサイトースで排泄すると言う働きがあります。
■肥満
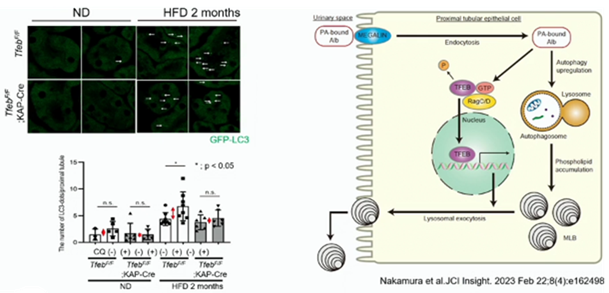
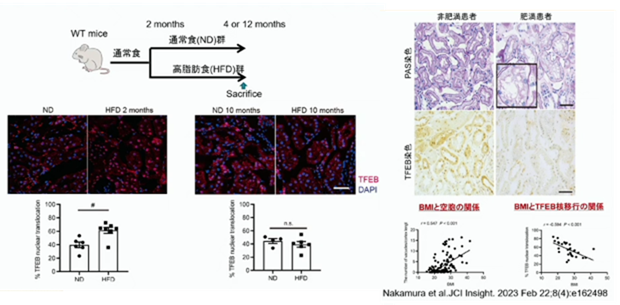
それでは高脂肪食を食べているとTEFBが亢進して良いのかと言うと、このワイドタイプのものに対して、通常食と高脂肪食を長期間に亘って食べさせていると、高脂肪食2ヶ月の段階では、まだTFEBは亢進しています。
しかしながら、10か月も続くと、TFEBの亢進が抑制されて、核内に移行が滞って来ます。肥満の人と肥満でない人を比べると、肥満の人はTFEBの発現が抑制されて来ます。高脂肪食を食べている、或いは肥満の人は、やはり短期間ではなく長期間同じような状態が続くと、TFEBの核移行がだんだん疲労して、減少してきて、上手く働くなって来てしまう。まあ、今時の、静かなる退職の様な状況に陥ります。下図を見てもらえれば明らかな様に、肥満患者さんでは、空胞病変が増加し、TFEB核内減少を認めます。
多機能性細胞間シグナル因子である線維芽細胞増殖因子(FGF)は、22種類存在し、夫々独自の生理的意義を有しています。その一つであるFGF21は、肥満症や肥満症を発症基盤とする糖脂質代謝異常を改善する薬理作用を持つ為、医学薬学分野に於いて注目を集めており、医療への応用を目指した研究が世界中で進められているホットな因子です。このFGF21も、オートファジーに関連しています。両者は協調的に働き、加齢や肥満に伴う腎臓病に対抗します。
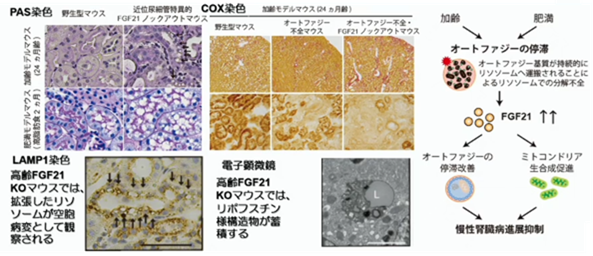
近位尿細管に特異的なFGF21ノックアウトマウスに、肥満モデルとして高脂肪食を投与していると、尿細管細胞にリソソームの蓄積が認められるようになります。また加齢マウスで見てみると、オートファジー不全マウスとFGF21のノックアウトマウスを掛け合わせると、ミトコンドリアの機能が非常に低下して来ます。加齢や肥満は、オートファジーの停滞を促します。FGF21は、オートファジーの停滞を改善する、或いはミトコンドリアの生合成を促進する事によって、慢性腎臓病の進展を抑制してくれます。しかし、FGF21の機能も低下すると、両者が相まって、腎臓病が進行してしまいます。
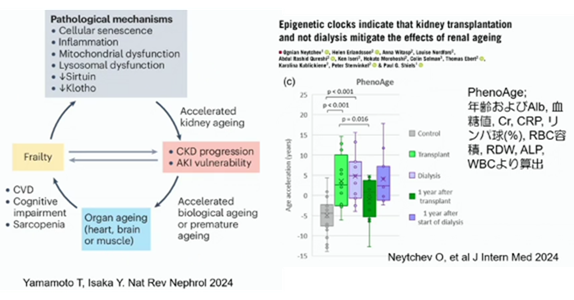
腎臓の老化は全身の老化を促進
慢性腎臓病は、全身の老化を促進して、まあ例えばフレイルであったり、心臓病を促進します。例えば、腎臓の移植を行うと、透析に比べて、Pheno因子と言う老化の指標ですが、抑制されされます。腎臓を移植によって若返らせると、全身の老化も抑制されるのではと推測されます。
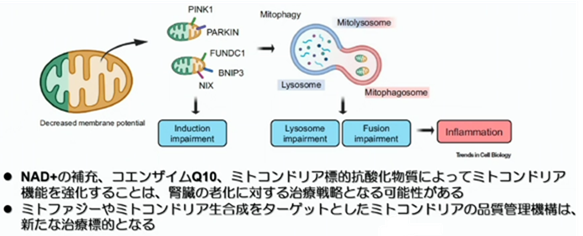 ミトコンドリアは老化と関連していますが、NAD、CoQ10、ミトコンドリア標的抗酸化物質によってミトコンドリアの機能を強化する事は、老化を抑制する事に繋がります。
ミトコンドリアは老化と関連していますが、NAD、CoQ10、ミトコンドリア標的抗酸化物質によってミトコンドリアの機能を強化する事は、老化を抑制する事に繋がります。
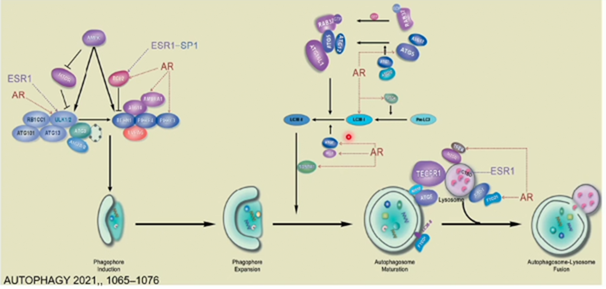 また、性差にも関連しますが、性ホルモンもオートファジー制御に重要な要因です。アンドロゲン受容体ARもオートファジーと関連しており、この制御も重要になります。
また、性差にも関連しますが、性ホルモンもオートファジー制御に重要な要因です。アンドロゲン受容体ARもオートファジーと関連しており、この制御も重要になります。
様々なオートファジーの機能を制御する事によって、これ等の治療の可能性があると思われます。
老化を起こさせるメカニズム、長寿を支えるメカニズムを解明する為に、日々研究者はこんな苦労をしている
種間比較トランスクリプトミクスによる寿命制御メカニズムの解明
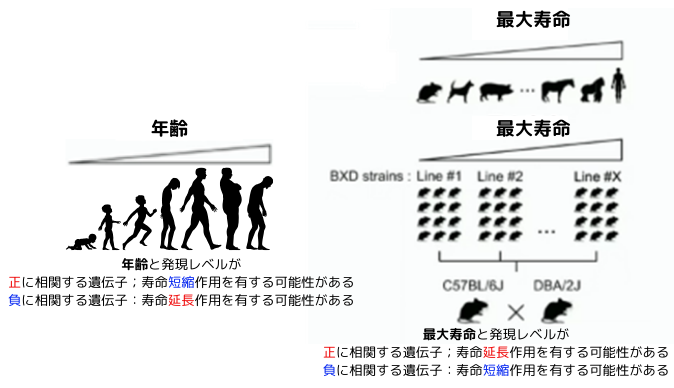 老化を起こさせるメカニズムがあります。一方、長寿を支えるメカニズムもあり、この2つは別物です。
老化を起こさせるメカニズムがあります。一方、長寿を支えるメカニズムもあり、この2つは別物です。
年齢と発現レベルが、①正に相関する遺伝子=寿命短縮作用を有する可能性があると、②負に相関する遺伝子=寿命延長作用を有する可能性があるの2つの遺伝子に大きく分けられます。また、最大寿命と発現のレベルが、①正に相関する遺伝子=寿命延長作用を有する可能性があると、②負に相関する遺伝子=寿命短縮作用を有する可能性があるの2つの遺伝子に大きく分けられます。つまり、加齢と相関する遺伝子、最大寿命と相関する遺伝子は、反対の性質を帯びているのではないかと思われがちですが、しかしながら、実際には、そう単純な話ではなくて、老化に伴って起きる事は全て悪い事ではありません。
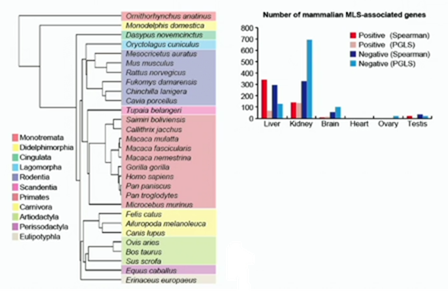 これを検証する為に、先ずは29種類の、哺乳類の最大寿命と相関する遺伝子を抽出しました。肝臓や腎臓等の代謝に強く関連する組織で、長寿と相関する遺伝子が多く検出されました。精巣でもそれなりには検出出来ましたが、卵巣では殆ど検出出来ませんでした。
これを検証する為に、先ずは29種類の、哺乳類の最大寿命と相関する遺伝子を抽出しました。肝臓や腎臓等の代謝に強く関連する組織で、長寿と相関する遺伝子が多く検出されました。精巣でもそれなりには検出出来ましたが、卵巣では殆ど検出出来ませんでした。
 上の図を見て下さい。長寿と相関している遺伝子をピックアップしてみました。縦軸は遺伝子の発現レベル。横軸は、2つセットのペアで、左側が最大寿命と発現レベルとの相関、右側が発現レベルと年齢の相関を表しています。赤で囲った加齢に伴い発現が上昇する免疫/炎症関連遺伝子では、例えば、CD4がこれに相当しますが、年齢と最大寿命の両方で正の相関を示している、つまり、長寿の哺乳動物でより高く発現している傾向がありました。一方、青で囲んだ、加齢に伴い発現が低下するミトコンドリアに関わる遺伝子は、長寿の哺乳動物でより低く発現している傾向が認められました。
上の図を見て下さい。長寿と相関している遺伝子をピックアップしてみました。縦軸は遺伝子の発現レベル。横軸は、2つセットのペアで、左側が最大寿命と発現レベルとの相関、右側が発現レベルと年齢の相関を表しています。赤で囲った加齢に伴い発現が上昇する免疫/炎症関連遺伝子では、例えば、CD4がこれに相当しますが、年齢と最大寿命の両方で正の相関を示している、つまり、長寿の哺乳動物でより高く発現している傾向がありました。一方、青で囲んだ、加齢に伴い発現が低下するミトコンドリアに関わる遺伝子は、長寿の哺乳動物でより低く発現している傾向が認められました。
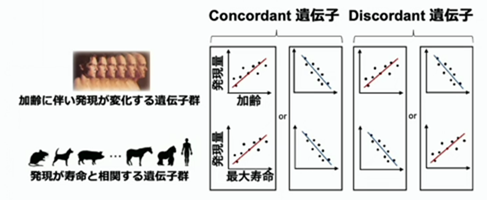 種内で加齢に伴い発現が変化する遺伝子群と、種間で発現が寿命が相関する遺伝子群は良く似ています。
種内で加齢に伴い発現が変化する遺伝子群と、種間で発現が寿命が相関する遺伝子群は良く似ています。
先に用語の定義を説明しますが、加齢に伴い発現が変化する遺伝子群と、寿命と相関する遺伝子群を考えた時に、どちらの遺伝子群でも、正の相関を示す遺伝子は合致した挙動を示すので、Concordant(=合致する)遺伝子とします。加齢に伴い下がるし、長寿動物で下がると言う合致した挙動を示す遺伝子も、Concordant遺伝子とします。一方反対の挙動を示す遺伝子を、Discordant(=不一致)遺伝子と定義しました。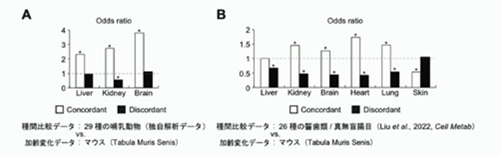 解析の結果、2つの遺伝子群が全く無関係だとした際に、それでも一定のオーバーラップは考えられますが、全く無関係だと仮定した場合の、Concordant遺伝子がOdds比が押しなべて1よりも大きくなりました。つまり、似てる傾向が多かったんです。反対の性質を帯びている遺伝子がどれくらいあるかと言うと、Odds比が有意に1よりも低いケースが散見されました。全体的に、老化すると機能は低下しますが、しかし、ある一側面を見ると、そうではなくて、長寿動物化しているんだよ!とも言えます。
解析の結果、2つの遺伝子群が全く無関係だとした際に、それでも一定のオーバーラップは考えられますが、全く無関係だと仮定した場合の、Concordant遺伝子がOdds比が押しなべて1よりも大きくなりました。つまり、似てる傾向が多かったんです。反対の性質を帯びている遺伝子がどれくらいあるかと言うと、Odds比が有意に1よりも低いケースが散見されました。全体的に、老化すると機能は低下しますが、しかし、ある一側面を見ると、そうではなくて、長寿動物化しているんだよ!とも言えます。
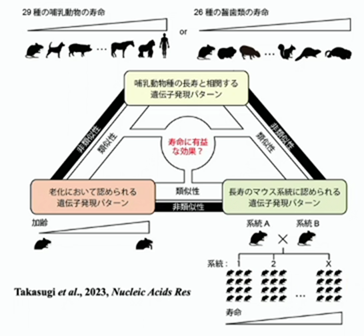 種間比較ではなくて、マウスに限るお話ですが、マウスにも系統が何十、何百もあり、寿命が長いもの、短いものもあります。寿命が長い程発現が高い遺伝子は、老化関連遺伝子と類似しており、加齢変動遺伝子ではありますが、適応的な老化を制御している遺伝子が多く含まれています。
種間比較ではなくて、マウスに限るお話ですが、マウスにも系統が何十、何百もあり、寿命が長いもの、短いものもあります。寿命が長い程発現が高い遺伝子は、老化関連遺伝子と類似しており、加齢変動遺伝子ではありますが、適応的な老化を制御している遺伝子が多く含まれています。
例えば、加齢に伴い脳で発現が低下し、その事が保護的な役割を発揮するREST(repressor element 1 silencing transcription factor)って転写抑制因子で、認知機能の保持に貢献しています。Tao Luらによれば、若い人の脳のニューロンでは通常殆ど発現していないRESTが、高齢者の脳では非常に高レベルに発現している事、そして、軽度認知障害(しばしば、認知症に先行する症状)がある人とアルツハイマー病患者のニューロンの核では、RESTの発現レベルが著しく低下していることを明らかにしました。Luらは更に、以前に神経精神病学的評価を受けた人々の前頭前皮質の死後サンプルを分析し、ニューロンの核でのRESTレベルと認知機能との間に正の相関が見られる事を発見しました。こうした知見を総合すると、認知機能低下とアルツハイマー病の予防には、加齢脳でREST蛋白質の発現レベルを維持する事が重要と考えられます。
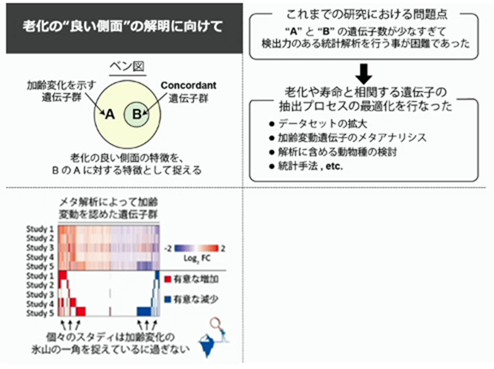 老化の良い側面の解明に向けて、具体的なアプローチとしては、加齢変動遺伝子全体をAとした時に、その中に含まれる適応的な老化と思しきConcordant遺伝子群Bとします。Aに対するBの特徴を明らかにして、老化の良い側面を明らかにしていく。しかし、遺伝子数が少な過ぎて、検出力のある解析が行えな得ない状況が往々にしてありました。そこで、老化や寿命と相関する遺伝子の抽出プロセスの最適化って名前の、ずるっこの手法を解説します。例えば、メタアナリシスを行って解析プロセスを見直します。どういう事かと言えば、例えば、骨格筋の加齢変動を報告した5つの論文があるとします。殆ど同じマウスの系列の同じ週齢のマウスを比べた報告になりますが、個々の研究で発現が有意に上がった/下がったと言う遺伝子はあまりオーバーラップしていません。あまり数も取れていません。しかし、この研究1~5までを含めてメタ解析すると、ここからここまでは増えている遺伝子、ここからここまでは減っている遺伝子と、加齢変動を認める遺伝子が増えます。従来、夫々の研究では、強く現れている部分だけを注目してしまうんですが、メタ解析を行う事で、老化の全体像を見る事がかのうになります。人だとnを多く取る事が出来ますが、マウスでは精々3とか5とか…nを多く設定する事が難しいいケースが多いんです。だからマウスであるからこそ、メタ解析≒ずるっこ解析が重要になって来るんですね(笑)。
老化の良い側面の解明に向けて、具体的なアプローチとしては、加齢変動遺伝子全体をAとした時に、その中に含まれる適応的な老化と思しきConcordant遺伝子群Bとします。Aに対するBの特徴を明らかにして、老化の良い側面を明らかにしていく。しかし、遺伝子数が少な過ぎて、検出力のある解析が行えな得ない状況が往々にしてありました。そこで、老化や寿命と相関する遺伝子の抽出プロセスの最適化って名前の、ずるっこの手法を解説します。例えば、メタアナリシスを行って解析プロセスを見直します。どういう事かと言えば、例えば、骨格筋の加齢変動を報告した5つの論文があるとします。殆ど同じマウスの系列の同じ週齢のマウスを比べた報告になりますが、個々の研究で発現が有意に上がった/下がったと言う遺伝子はあまりオーバーラップしていません。あまり数も取れていません。しかし、この研究1~5までを含めてメタ解析すると、ここからここまでは増えている遺伝子、ここからここまでは減っている遺伝子と、加齢変動を認める遺伝子が増えます。従来、夫々の研究では、強く現れている部分だけを注目してしまうんですが、メタ解析を行う事で、老化の全体像を見る事がかのうになります。人だとnを多く取る事が出来ますが、マウスでは精々3とか5とか…nを多く設定する事が難しいいケースが多いんです。だからマウスであるからこそ、メタ解析≒ずるっこ解析が重要になって来るんですね(笑)。
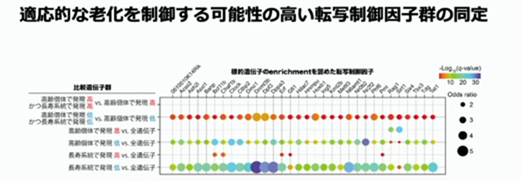 現在、適応的な老化を制御する可能性の高い転写因子群の同定まで進んでいます。
現在、適応的な老化を制御する可能性の高い転写因子群の同定まで進んでいます。
プロテオーム/マトリソーム
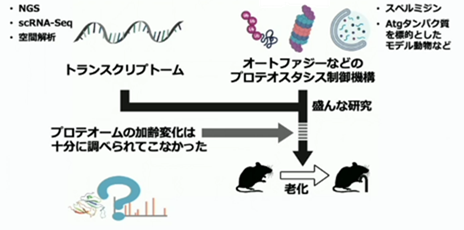 トランスクリプトームやプロテオスタシス制御に注目した研究が流行りではありますが、プロテオームの加齢変化は未だ大部分が解明されていません。
トランスクリプトームやプロテオスタシス制御に注目した研究が流行りではありますが、プロテオームの加齢変化は未だ大部分が解明されていません。
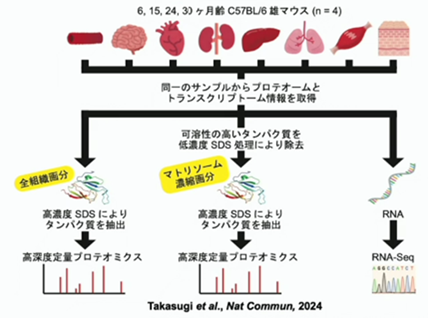 手始めに、マウスのエイジングのproteomic atlasを構築してみました。マウスの24ヶ月齢は、ヒトで言うと60代後半に該当します。未だ、(後期)高齢者医療受給者証をもらえる年齢ではないので、30ヶ月齢のマウスも含めて、同じ組織粉末を使って、トランスクリプトームデータを取りました。更に可溶性の高い蛋白質をウォッシュアウトして、残った膜蛋白質や細胞外マトリックスが濃縮されたマトリソームの濃縮画分に対しても、プロテオミクス解析を行いました。
手始めに、マウスのエイジングのproteomic atlasを構築してみました。マウスの24ヶ月齢は、ヒトで言うと60代後半に該当します。未だ、(後期)高齢者医療受給者証をもらえる年齢ではないので、30ヶ月齢のマウスも含めて、同じ組織粉末を使って、トランスクリプトームデータを取りました。更に可溶性の高い蛋白質をウォッシュアウトして、残った膜蛋白質や細胞外マトリックスが濃縮されたマトリソームの濃縮画分に対しても、プロテオミクス解析を行いました。
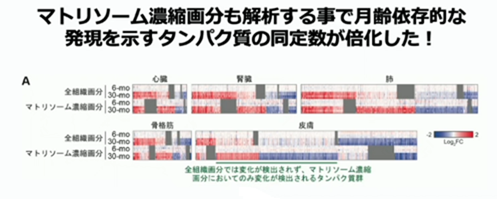
こんなちょっとした工夫を加えるだけで、マトリソーム濃縮画分の解析についてですが、月齢依存的に発現を示す蛋白質の同定数が倍加しました。特に特徴的であったのは、例えば皮膚のマトリソーム濃縮分画では、加齢に伴って増加したり減少したりと変動する遺伝子もありますが、全く加齢性の変化が認められないものもあります。同じ細胞組織の、同じ蛋白質の中でも、活性が低いものは、加齢性の変化を起こしやすい事が分かっています。
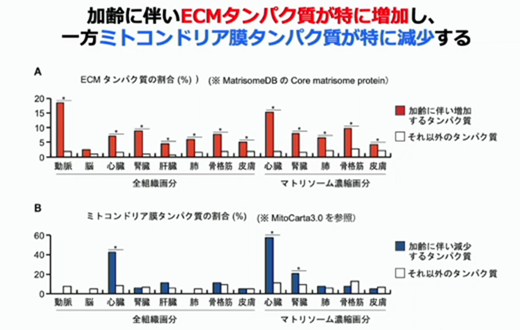
細胞外マトリックスの蛋白質は、加齢による変化が一番認められやすい蛋白質でもあります。右図では、加齢に伴い増加する蛋白質を赤で示していますが、ECM蛋白質の割合が高くなっており、それ以外の蛋白質は2~3%、1~2%くらいしかありません。例えば、動脈であれば、加齢に伴い増加する蛋白質の20%くらいをECM蛋白質が占めています。全組織分画でもマトリソーム濃縮分画でもこの様な傾向が認められており、平均で5倍くらいのエンリッチメントがありました。逆に、加齢に伴って減る蛋白質では、全ての組織で共通する特徴はありませんが、特に心臓で、次いで腎臓で、ミトコンドリアの膜蛋白質が顕著に減少していました。
 色んな組織で、加齢に伴いECM蛋白質が増加するのは、線維化が原因ではないのか? そんな疑問が浮かびます。しかし、加齢に伴って増えてくるECM蛋白質の種類は、組織によって異なっており、オーバーラップする部分は少ない。これは、全組織画分でもマトリソーム濃縮分画でも、同様の傾向が認められました。また、線維性コラーゲンCol1a1、Col1a2,Col1a3は、減少するケースこそあれ、増加するケースは実はなくて、ここで見ている加齢性細胞外沈着物は一般的な線維化とは違います。どうもアミロイドーシスでもないみたいだし…。追って研究報告が待たれるところです。
色んな組織で、加齢に伴いECM蛋白質が増加するのは、線維化が原因ではないのか? そんな疑問が浮かびます。しかし、加齢に伴って増えてくるECM蛋白質の種類は、組織によって異なっており、オーバーラップする部分は少ない。これは、全組織画分でもマトリソーム濃縮分画でも、同様の傾向が認められました。また、線維性コラーゲンCol1a1、Col1a2,Col1a3は、減少するケースこそあれ、増加するケースは実はなくて、ここで見ている加齢性細胞外沈着物は一般的な線維化とは違います。どうもアミロイドーシスでもないみたいだし…。追って研究報告が待たれるところです。
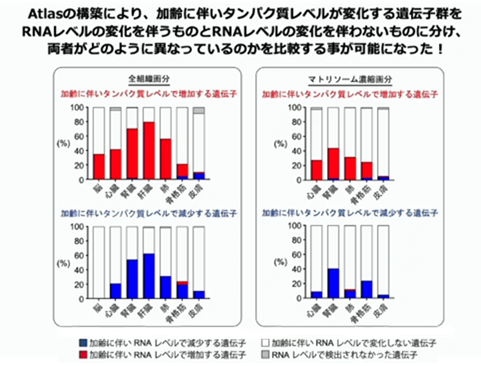 次にプロテームのデータとトランスフォームのデータを重ね合わせて、実際に両者がどれくらい合致しているのかを調べてみると、実はそれほど合致していませんでした。全組織画分で加齢に伴い蛋白質レベルで増加する遺伝子の中で、どれくらいの割合でRNAでも動いているのかを見てみると、例えば、心臓では加齢に伴って増える蛋白質の高だか40%くらいしか、RNAレベルでは有意に動いていない。つまり、やっぱりRNAの評価は重要なんだけれど、最終的に蛋白質を見るって事も重要だよねって事が分かって来ました。
次にプロテームのデータとトランスフォームのデータを重ね合わせて、実際に両者がどれくらい合致しているのかを調べてみると、実はそれほど合致していませんでした。全組織画分で加齢に伴い蛋白質レベルで増加する遺伝子の中で、どれくらいの割合でRNAでも動いているのかを見てみると、例えば、心臓では加齢に伴って増える蛋白質の高だか40%くらいしか、RNAレベルでは有意に動いていない。つまり、やっぱりRNAの評価は重要なんだけれど、最終的に蛋白質を見るって事も重要だよねって事が分かって来ました。
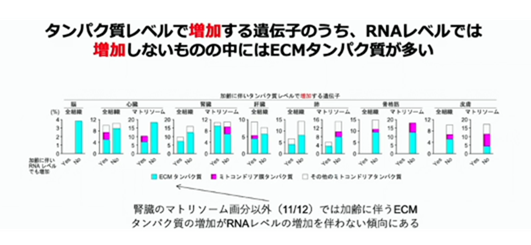 加齢に伴って蛋白質だけ動いてRNAでは動かないような蛋白質の存在が、今回の解析で初めて分かって来ました。この図は加齢に伴って増加する遺伝子ですが、RNAレベルでも増えるものYES、増えないものNOで分類してみると、RNAレベルでは増加しないもの中には、ECM蛋白質が多い事が分かりました。
加齢に伴って蛋白質だけ動いてRNAでは動かないような蛋白質の存在が、今回の解析で初めて分かって来ました。この図は加齢に伴って増加する遺伝子ですが、RNAレベルでも増えるものYES、増えないものNOで分類してみると、RNAレベルでは増加しないもの中には、ECM蛋白質が多い事が分かりました。
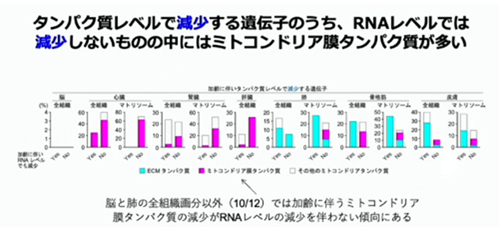 逆に、蛋白質レベルで減少する遺伝子のうち、RNAレベルでは減少しないものの中には、ミトコンドリア膜蛋白質が多い事が分かりました。実際、この中には、電子伝達系の蛋白質が、心臓に限らず様々な組織で、RNAの変化を伴わない形で蛋白質が減少しています。
逆に、蛋白質レベルで減少する遺伝子のうち、RNAレベルでは減少しないものの中には、ミトコンドリア膜蛋白質が多い事が分かりました。実際、この中には、電子伝達系の蛋白質が、心臓に限らず様々な組織で、RNAの変化を伴わない形で蛋白質が減少しています。
トピックス・話題の老化に対するワクチンって何?
ジェロサイエンス仮説は、老化そのものが、慢性疾患や加齢関連疾患の根本の原因であるとする仮説です。老化は細胞レベルで始まり、老化細胞が蓄積する事で臓器全体が老化し、加齢関連疾患が進行します。以前は、老化への医学的介入は不可能と考えられていましたが、研究の進歩に伴い、老化は避けられないものではなく、介入により遅らせる可能性が見出されるようになって来ました。即ち、老化を治療する事で、健康寿命を延ばす道が開かれつつあります。その代表格が、老化細胞除去治療(セノリシス)、別名・老化ワクチンです。
細胞老化
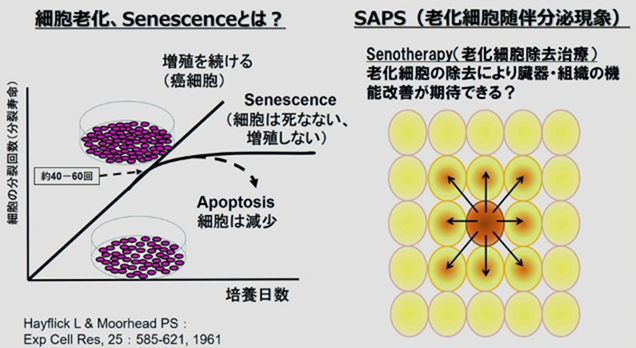 今話題の、細胞老化(senescece)ってご存じでしょうか? 細胞培養を行っていると、最初の頃は生きが良くて細胞はどんどん増えるんですが、パッセージを繰り返すと増えが徐々に悪くなって、そのうちメディオを変えても増えなくなって来ます。増殖はしないけど、死なない=Senescenceって状態になります。1961年にHayflickらによって発見されました。この様な細胞分裂の限界は、ヘイフリック限界とも呼ばれ、細胞が分裂寿命を迎えた事によって起こる細胞老化を、特に分裂老化と言います。
今話題の、細胞老化(senescece)ってご存じでしょうか? 細胞培養を行っていると、最初の頃は生きが良くて細胞はどんどん増えるんですが、パッセージを繰り返すと増えが徐々に悪くなって、そのうちメディオを変えても増えなくなって来ます。増殖はしないけど、死なない=Senescenceって状態になります。1961年にHayflickらによって発見されました。この様な細胞分裂の限界は、ヘイフリック限界とも呼ばれ、細胞が分裂寿命を迎えた事によって起こる細胞老化を、特に分裂老化と言います。
この細胞老化の主な原因として、細胞分裂が起こると、染色体末端にあるテロメア(美容通信2024年9月号)の短縮が起こりますが、一定の範囲を超えて短縮すると、DNA損傷として認識され、細胞増殖が停止すると言う事が明らかになりました。その後、2000年代に入り、細胞老化には分裂老化の他に、酸化ストレスや癌遺伝子の活性化、放射線や紫外線、炎症性サイトカイン等の様々なストレスによっても、細胞老化が誘発される事が分かって来ました。
2008年になり、老化細胞から炎症性サイトカイン、ケモカイン、増殖因子等を含んだSASP(senescence-associated secretory phenotype)が分泌され、周辺の正常細胞に影響を与えている事が明らかになりました。老化細胞随伴分泌現象(SAPS)とは、組織の中に1個老化が進んだ細胞があると、その周りの細胞はどんどん老化していく。Senescenceって状態は、一個悪い奴を取り除けば、周りは年を取るのが遅くなって、所謂組織の老化、固体老化は抑制出来るのではないか? つまり、テレビドラマ「3年B組金八先生」の中で語られた有名な概念、「腐ったミカンの方程式」です。この方程式は、一つの腐ったミカンが他のミカンを腐らせるという比喩で、組織や集団内の悪影響を示しており、老化に対するワクチンを理解する上で、重要となります。
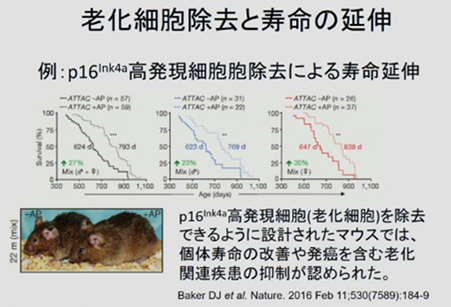 2011年、Bakerらは、老化した細胞を取り除く老化細胞除去「セノリシス(senescence + lysis)」と言う新しい老化治療の概念を提唱しました。左図は、p16と言う老化細胞のマーカーを発現した細胞、つまり腐ったミカンを取り除いたら、寿命が延びたという論文です。この結果を受け、セノリシスは新たな抗老化治療として注目を集め、老化細胞を標的としたセノリティクス薬(老化細胞特異的に細胞死を誘導する薬剤)やセノモルフィクス薬(老化細胞の機能を抑制し、SASPを阻害する薬剤)に関する研究が世界中で盛んに行われるようになりました。
2011年、Bakerらは、老化した細胞を取り除く老化細胞除去「セノリシス(senescence + lysis)」と言う新しい老化治療の概念を提唱しました。左図は、p16と言う老化細胞のマーカーを発現した細胞、つまり腐ったミカンを取り除いたら、寿命が延びたという論文です。この結果を受け、セノリシスは新たな抗老化治療として注目を集め、老化細胞を標的としたセノリティクス薬(老化細胞特異的に細胞死を誘導する薬剤)やセノモルフィクス薬(老化細胞の機能を抑制し、SASPを阻害する薬剤)に関する研究が世界中で盛んに行われるようになりました。
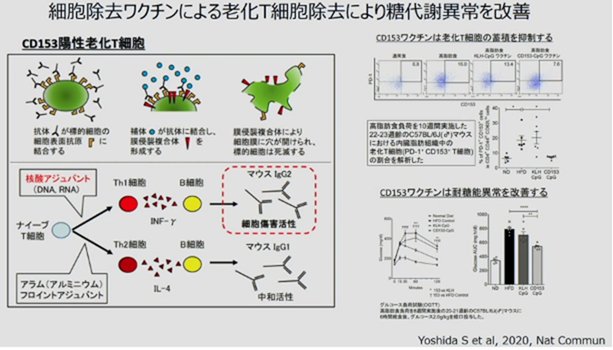
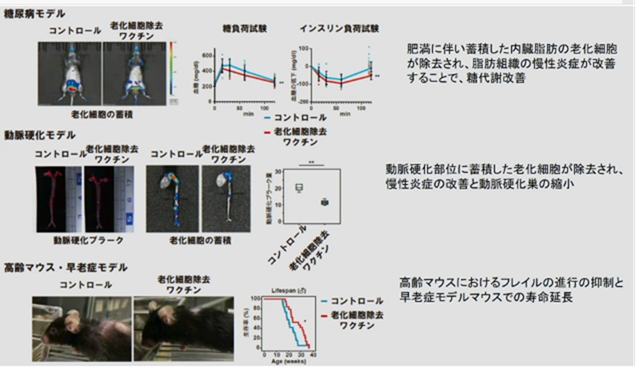
ワクチンで老化T細胞を除去する。厳密に言えば、老化T細胞の中のCD153ってマーカーを発現する細胞を取り除いているだけなので、完全に老化T細胞を除去したって訳ではありません。しかし、糖尿病の時に、脂肪で老化T細胞が増えて悪さをする事は知られており、これを取り除くと、糖尿病が改善します。
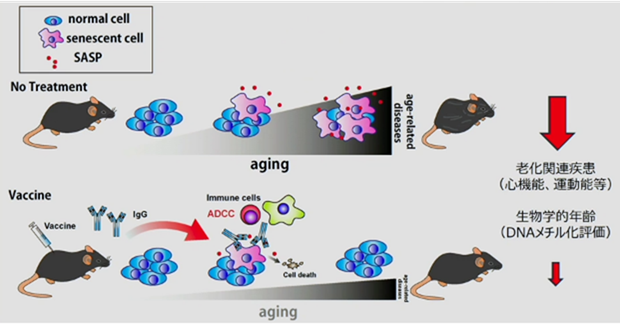
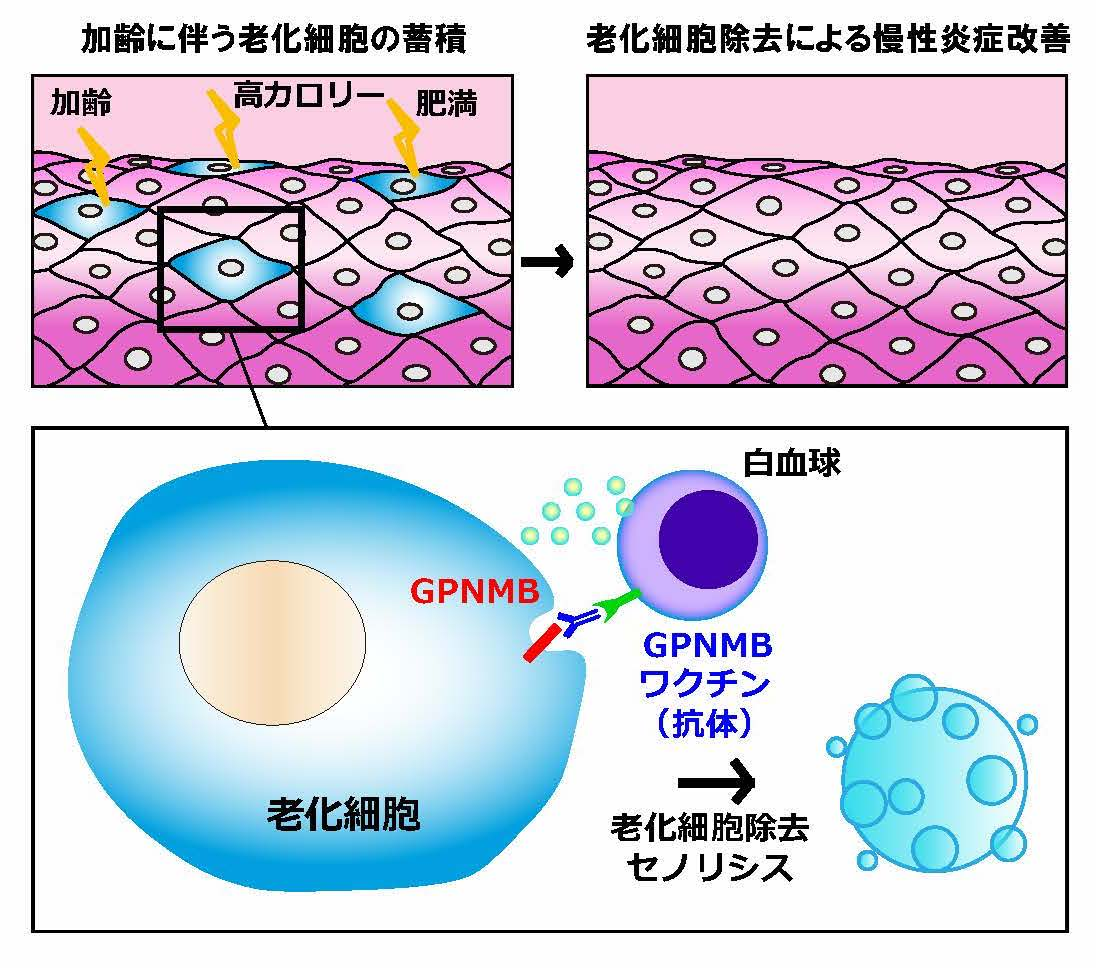 右図は、老化細胞除去ワクチンの作用メカニズムを示したものです。老化細胞を取り除く≒老化抗原の陽性細胞を取り除く。老化細胞除去ワクチンよって誘導される抗体による免疫反応により、老化細胞が選択的にセノリシスにより除去され、慢性炎症が改善され、糖尿病も良くなって、動脈硬化も良くなって、寿命も延びます。人間では色々な倫理上の問題等が山積していますが、マウスでは既に技術的に可能になっています。
右図は、老化細胞除去ワクチンの作用メカニズムを示したものです。老化細胞を取り除く≒老化抗原の陽性細胞を取り除く。老化細胞除去ワクチンよって誘導される抗体による免疫反応により、老化細胞が選択的にセノリシスにより除去され、慢性炎症が改善され、糖尿病も良くなって、動脈硬化も良くなって、寿命も延びます。人間では色々な倫理上の問題等が山積していますが、マウスでは既に技術的に可能になっています。
 村上龍の「歌うクジラ」を、久し振りに本棚から引き摺り出して、読み返しています…。
村上龍の「歌うクジラ」を、久し振りに本棚から引き摺り出して、読み返しています…。
関連ページ
関連するHISAKOの美容通信をピックアップしました。
来月号の予告
性差のエビデンスと最近の話題についての特集です。
<性差医学>