HISAKOの美容通信2024年2月号
皮膚微生物叢を操って、アトピー性皮膚炎や尋常性乾癬等の炎症性皮膚疾患を治療する新時代が到来!?
 炎症下のみならず、定常時に於いても、皮膚マイクロバイオームは皮膚免疫細胞とのクロストークを介して、皮膚の恒常性維持に貢献しています。皮膚マイクロバイオームの破綻は、獲得免疫応答の誘導等を介して、アトピー性皮膚炎や乾癬等の様々な炎症性皮膚疾患の病態に関与しています。マイクロマイオームを起点とする皮膚炎悪化のメカニズムを逆手に取った、従来の抗炎症治療とは一線を画す治療方法が、今後の治療の主流となるかも知れません。実験のレベルで、未だ確立された治療方法ではありませんが、例えば、アトピー性皮膚炎の治療として、黄色ブドウ球菌に対して、殺菌作用及び毒素抑制作用を有する人間の皮膚常在菌株を細菌移植する方法等も試み始められています。糞便微生物移植法の皮膚バージョンです。
炎症下のみならず、定常時に於いても、皮膚マイクロバイオームは皮膚免疫細胞とのクロストークを介して、皮膚の恒常性維持に貢献しています。皮膚マイクロバイオームの破綻は、獲得免疫応答の誘導等を介して、アトピー性皮膚炎や乾癬等の様々な炎症性皮膚疾患の病態に関与しています。マイクロマイオームを起点とする皮膚炎悪化のメカニズムを逆手に取った、従来の抗炎症治療とは一線を画す治療方法が、今後の治療の主流となるかも知れません。実験のレベルで、未だ確立された治療方法ではありませんが、例えば、アトピー性皮膚炎の治療として、黄色ブドウ球菌に対して、殺菌作用及び毒素抑制作用を有する人間の皮膚常在菌株を細菌移植する方法等も試み始められています。糞便微生物移植法の皮膚バージョンです。
『きのこ会議』は、1922年に「九州日報」で発表された夢野久作の短編小説です。きのこの様な植物の世界だけでなく、皮膚にも微生物叢あり、会議三昧の日々を過ごしているようです。今月号の美容通信では、最近の知見を基に、断片的ではありますが、会議の様子をご報告する事にしました。
毛嚢・脂腺が形成する免疫ハブ
 哺乳類に特有な構造である毛嚢と脂腺は、毛や皮脂で、皮膚を外的刺激から保護しています。あの手この手で生体内に侵入し増殖を試みる微生物どもに対して、私達生体は、幾重にも重なる免疫防御ラインを構築して強固な防衛に徹しています。しかし、今の岸田政権を見るまでもなく、防衛費は鰻登りに嵩みますし、下手すれば、支持率が下落し、自分自身が大怪我をする羽目に落ちります。妥協の産物ではありませんが、私達は、国益は異なれど、病原性が低いと判断される微生物と共存関係を持続する道を選ばざる得ません。北大西洋条約機構みたいなもんです。長い進化の過程で、越後谷と悪代官の関係とでも言いますか…持ちつ持たれつ、微生物叢は宿主の正常な免疫機能を維持する為には欠く事の出来ないパートナーに昇格しました。
哺乳類に特有な構造である毛嚢と脂腺は、毛や皮脂で、皮膚を外的刺激から保護しています。あの手この手で生体内に侵入し増殖を試みる微生物どもに対して、私達生体は、幾重にも重なる免疫防御ラインを構築して強固な防衛に徹しています。しかし、今の岸田政権を見るまでもなく、防衛費は鰻登りに嵩みますし、下手すれば、支持率が下落し、自分自身が大怪我をする羽目に落ちります。妥協の産物ではありませんが、私達は、国益は異なれど、病原性が低いと判断される微生物と共存関係を持続する道を選ばざる得ません。北大西洋条約機構みたいなもんです。長い進化の過程で、越後谷と悪代官の関係とでも言いますか…持ちつ持たれつ、微生物叢は宿主の正常な免疫機能を維持する為には欠く事の出来ないパートナーに昇格しました。
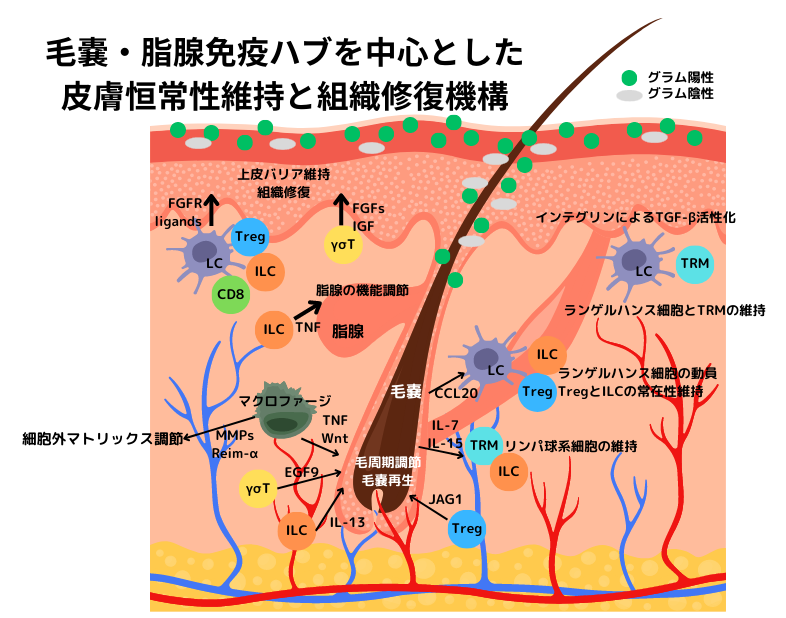
近年、毛嚢と脂腺は、免疫細胞を皮膚に定着させ、育む為の重要な場所を提供する、謂わば免疫ハブとして機能している事が分かって来ました。免疫細胞の中でも、特に、自然免疫に属するリンパ球系の細胞、自然リンパ球(innate lymphoid cells)は、恒常的な皮膚バリアと皮膚常在微生物叢の維持に重要と考えられています。
毛嚢・脂腺と免疫システム
免疫細胞が皮膚の細菌叢と出会う事が、病原体に対する防衛機構や創傷治癒(美容通信2004年5月号)等に必要な機能の獲得、維持に欠かす事が出来ません。しかし、細菌叢の構成バランスの異常であるディスバイオーシスが一旦起こってしまうと、一蓮托生的に、そのとばっちりが免疫細胞の機能にもがっちり及んでしまいます。
毛嚢や脂腺は、様々な免疫細胞とインタラクションを行う事で、皮膚バリアの恒常性を保つ上で重要な役割を担っています。多くの報告から、上図の如くに、毛嚢周囲に免疫細胞が集積し、これらが毛嚢から産生されるケモカインやサイトカイン等の液性因子によって制御されている事が分かっています。例えば、皮膚にはケモカインレセプターCCR6を発現する様々な細胞が存在しますが、これ等は毛嚢が産生するCCL20によって、毛嚢周囲に集って来ます。CCL20は、皮膚バリアの最前線で待機し、侵入を図る抗原どもを補足するランゲルハンス細胞と、過度な免疫反応を抑える事で組織の免疫バランスを整える制御性T細胞(Tree)の組織動態を左右しています。しかしながら、実は、このCCL20の首根っこを押さえているのが常在細菌どもなんです。
最近になって、制御性T細胞(Tree)は、その名の通り免疫抑制がお仕事と考えられていましたが、それだけでなく、毛の発育や線維芽細胞の増殖にも関わっている事が分かって来ました。Treeのみならず、組織常在性の免疫細胞達も、私達が単に無知で知らなかっただけで、皮膚の強固な防衛に関わる地球防衛軍の大事な一員だったんですね。
組織恒常性維持を担う自然リンパ球
■皮膚マイクロバイオーム調節
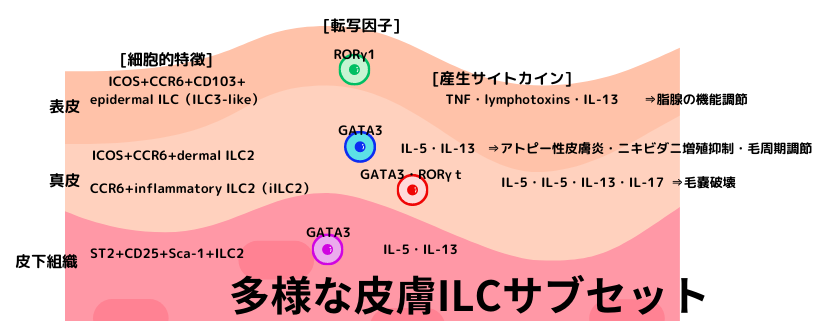
これまで、リンパ球系の自然免疫細胞としては、ウイルス感染や癌免疫に係るNK細胞が知られていましたが、近年、それ以外のリンパ球系免疫細胞も様々な組織に常在している事が明らかになって来ました。彼らは、自然リンパ球innate lymphoid cellsと名付けられ、皮膚に於いても、微生物感染と言う生物にとって危機的な状況のみならず、定常状態に於いても、微生物叢の制御と密接な関りを持っている事が分かって来ました。自然リンパ球は3グループに分類され、①NK細胞及びグループ1(ILC1)は、IFNγやTNF等を産生し、ウィルスや細菌感染細胞等の排除を担当します。②グループ2自然リンパ球(ILC2)は、寄生虫感染や組織修復、アレルギー病態に係る細胞で、IL-33やTSLP、IL-25によって活性化され、IL-5やIL-13等の2型サイトカインを産生します。③グループ3自然リンパ球(ILC3)は、IL-17やIL-22を産生し、細胞外細菌感染の際に働きます。
脂腺からは多様な皮脂成分が常時垂れ流されていて、皮膚の表面を覆って乾燥を防ぐと共に、その抗菌的な作用により病原体の感染を防いでいます。しかし、抗菌脂質の過剰な分泌は、皮膚常在細菌叢のバランスを崩す大きな原因となるので、自然リンパ球はこの様な事態を避ける為、毛嚢、特に脂腺の周囲に集って、皮脂の機能を適切に調節していると考えられています。つまり、自然リンパ球には、皮膚のマイクロバイオームを維持し、恒常性を支えている役割があるようです。
■寄生虫増殖抑制
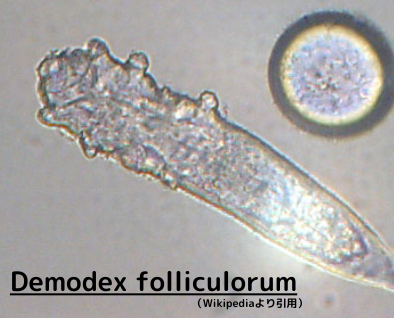 勿論、皮膚の上に棲息しているのは細菌だけはありません。寄生虫もいます。例えば、ニキビダニは毛嚢内に住居を構える常在の寄生虫で、普通の状態では私達に何ら害を及ぼすなんて事もないんですが、阿呆みたいに増えて炎症反応を起こして、毛嚢炎や酒さの原因の一つとなります。最近、皮膚のIL-13を産生する自然リンパ球であるILC2が、ニキビダニの増殖を押させる働きをしている事が明らかになりました。ILC2が産生するIL-4やIL-13等の2型サイトカインは、毛嚢の幹細胞に働きかける事で、毛の再生を調節し、毛嚢内に寄生するニキビダニの増殖を抑えていたんです。
勿論、皮膚の上に棲息しているのは細菌だけはありません。寄生虫もいます。例えば、ニキビダニは毛嚢内に住居を構える常在の寄生虫で、普通の状態では私達に何ら害を及ぼすなんて事もないんですが、阿呆みたいに増えて炎症反応を起こして、毛嚢炎や酒さの原因の一つとなります。最近、皮膚のIL-13を産生する自然リンパ球であるILC2が、ニキビダニの増殖を押させる働きをしている事が明らかになりました。ILC2が産生するIL-4やIL-13等の2型サイトカインは、毛嚢の幹細胞に働きかける事で、毛の再生を調節し、毛嚢内に寄生するニキビダニの増殖を抑えていたんです。
■ディスバイオーシスに端を発した毛嚢破壊
また、ディスバイオーシスとそれに伴う炎症性のILC2浸潤は、毛嚢を破壊し、脱毛の原因になるとの報告もあります。細菌叢バランスの乱れは、自然免疫系の暴走と組織破壊を招きます。
■皮膚バリア機能の維持
自然リンパ球サブセットは、機械的な刺激で損なわれてしまった皮膚のバリアを修復する過程に於いても、重要な役割を果たしています。バリア機能の破壊は、常在細菌叢のバランスを乱す大きな要因の一つですから、一大事! 自然リンパ球は常に監視の目を光らせていて、損傷した皮膚から発せられるSOS信号であるデンジャーシグナルを素早く感知すると、上皮細胞の増殖、分化を促して皮膚の修復を図り、日々、恒常性の維持に努めているんです。
皮膚マイクロバイオームと獲得免疫
炎症下のみならず、定常時に於いても、皮膚マイクロバイオームは皮膚免疫細胞とのクロストークを介して、皮膚の恒常性維持に貢献しています。皮膚マイクロバイオームの破綻は、獲得免疫応答の誘導等を介して、アトピー性皮膚炎や乾癬等の様々な炎症性皮膚疾患の病態に関与しています。マイクロマイオームを起点とする皮膚炎悪化のメカニズムを逆手に取った、従来の抗炎症治療とは一線を画す治療方法が、今後の治療の主流となるかも知れません。
尋常性乾癬
尋常性乾癬(美容通信2008年4月号)(美容通信2019年9月号)の病態の中心は、IL-17A/IL-23を基軸にした免疫応答です。また、尋常性乾癬の皮膚では、抗菌ペプチド、特にIL-37の発現が亢進しています。外的刺激により、ケラチノサイトから放出された自己由来のDNAとLL-37は複合体を形成し、形質細胞様樹状細胞からのインターフェロンαの産生を促進し、乾癬の症状を悪化させます。
■乾癬と皮膚マイクロバイオーム
尋常性乾癬と皮膚のマイクロバイオームとの関係については、未だ、完全に解明されている訳ではありません。しかし、尋常性乾癬の病変部では、細菌叢の多様性が失われており、また、普通はほぼ一択状態とされるマラセチアの真菌の割合が減る代わりに、Candida属の割合が増加している等、皮膚常在微生物叢のバランスの破綻(ディスバイオーシス)が病態に関与していると考えられています。
■尋常性乾癬に於ける皮膚常在真菌の役割
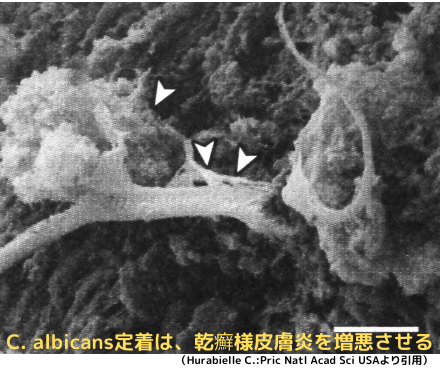 皮膚常在真菌は、真菌抗原特異的な免疫反応や好中球によるNETs形成を介して、病態の増悪に関与している可能性が示唆されています。
皮膚常在真菌は、真菌抗原特異的な免疫反応や好中球によるNETs形成を介して、病態の増悪に関与している可能性が示唆されています。
アトピー性皮膚炎
アトピー性皮膚炎(美容通信2007年4月号)(美容通信2019年7月号)(美容通信2020年12月号)は、乳児期に発症する強い痒みと慢性的な湿疹病変を特徴とする、Type2型免疫応答による慢性炎症性皮膚疾患です。Type2型免疫応答と同時に、アトピー性皮膚炎の皮膚ではバリア機能が著しく低下しており、その為、非特異的な刺激に対する被刺激性が亢進していると考えられています。
アトピー性皮膚炎の患者さんでは、症状の増悪時に皮膚細菌叢の構成が劇的に変化し、特に黄色ブドウ球菌の割合が顕著に増加しています。つまり、皮膚細菌叢のディスバイオーシスが、症状の増悪に関与しているものと思われます。
■黄色ブドウ球菌とアトピー性皮膚炎
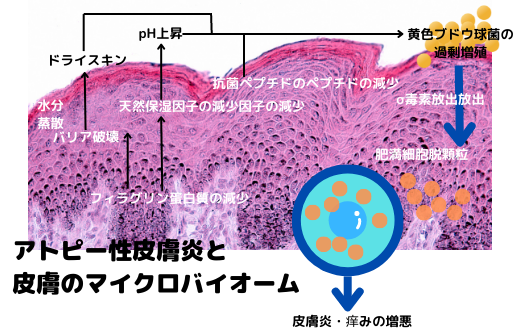 アトピー性皮膚炎の患者さんの皮膚からは、黄色ブドウ球菌が頻繁に分離される事は、大昔から知られていました。後述しますが、右図の如く、黄色ブドウ球菌の菌体外毒素による皮膚炎の増悪の可能性や、黄色ブドウ球菌の増殖からのディスバイオーシスによる正常細菌叢の破綻による皮膚炎の増悪等、徐々に黄色ブドウ球菌がアトピー性皮膚炎の病態にどの様に関与しているのかが解明されつつあります。
アトピー性皮膚炎の患者さんの皮膚からは、黄色ブドウ球菌が頻繁に分離される事は、大昔から知られていました。後述しますが、右図の如く、黄色ブドウ球菌の菌体外毒素による皮膚炎の増悪の可能性や、黄色ブドウ球菌の増殖からのディスバイオーシスによる正常細菌叢の破綻による皮膚炎の増悪等、徐々に黄色ブドウ球菌がアトピー性皮膚炎の病態にどの様に関与しているのかが解明されつつあります。
■マラセチアとアトピー性皮膚炎
成人のアトピー性皮膚炎の患者さんの皮膚からは、高確率にマラセチア、特に、M. globosa、M. restricaが検出され、健常人と比べて、分離される菌種が多く、量も多い事が知られていましたし、マラセチア特異的IgEも上昇している事は報告されていましたが、その詳細は未だ分かっていません。しかし、アトピー性皮膚炎の増悪因子である汗の中に含まれる、マラセチア由来の蛋白質抗原が、アトピー性皮膚炎の症状を増悪させるアレルギー反応を誘導している等、後述しますが、徐々に解明されつつはあります。
皮膚微生物間のコミュニケーション
外界と接する皮膚の表面には、細菌・ウィルス・真菌等の多彩な微生物が、コミュニティ(微生物叢)を形成しています。近年、次世代シークエンサーが登場し、皮膚は、外界の様々な微生物の侵入を物理的、化学的に阻んでいるだけでなく、皮膚表面をねぐらとする常在微生物達ともお互いに影響し合っている事が分かって来ました。微生物同士も、皮膚の表面で多彩な形でコミュニケーションを取り合う事で、微生物叢のバランスが形成され、それが皮膚の様々な疾患に関与している事も、知られるようになって来ました。最もよく研究が進んでいるのが、黄色ブドウ球菌のコミュニケーションツールであるクオセラムセンシング機構です。後述しますが、アトピー性皮膚炎の増悪に関与している事が分かっています。
 皮膚微生物叢とアトピー性皮膚炎を始めとする皮膚の病気の関係が解明が進んでいなかった時代は、病気を引き起こす若しくは増悪させる菌種をターゲットにした抗菌薬を使用して、病状を改善するしかありませんでした。尤もその前は、祈禱師に頼るしかありませんでしたが…。しかしながら、幾らターゲットにした菌を抗菌剤で駆除しようとしても、例えば、アトピー性皮膚炎の治療に抗菌剤を使用しても、その効果は一般的に乏しく、寧ろ、新たな耐性菌の出現の後押しをするだけのいたちごっこに終始していました。また、どの抗菌剤も、単一の菌や株だけを狙い撃ちして壊滅させるなんて芸当は不可能で、無暗な抗菌剤の乱用は、微生物叢の調和を乱し、将来的に予想だにしなかった災いが降りかかるやも知れません。
皮膚微生物叢とアトピー性皮膚炎を始めとする皮膚の病気の関係が解明が進んでいなかった時代は、病気を引き起こす若しくは増悪させる菌種をターゲットにした抗菌薬を使用して、病状を改善するしかありませんでした。尤もその前は、祈禱師に頼るしかありませんでしたが…。しかしながら、幾らターゲットにした菌を抗菌剤で駆除しようとしても、例えば、アトピー性皮膚炎の治療に抗菌剤を使用しても、その効果は一般的に乏しく、寧ろ、新たな耐性菌の出現の後押しをするだけのいたちごっこに終始していました。また、どの抗菌剤も、単一の菌や株だけを狙い撃ちして壊滅させるなんて芸当は不可能で、無暗な抗菌剤の乱用は、微生物叢の調和を乱し、将来的に予想だにしなかった災いが降りかかるやも知れません。
最近は、黄色ブドウ球菌を例に取れば、クオラムクエンチングシステムを利用して、他の菌株を塗布して黄色ブドウ球菌の病原性を抑える研究が大きな成果と注目を集めており、将来的な治療の主流となるやも知れません。
皮膚微生物叢間のコミュニケーション
■皮膚表面に於ける微生物の競合と共生
皮膚常在菌は、皮膚表面でコミュニティを形成する事によって、宿主である人に対して、有害な病原菌若しくは有害となりうる可能性がある日和見菌の定着や、病原性を抑える働きをしています。未だ、皮膚細菌叢の全容が解明されてはいませんが、細菌同士は、他の細菌の増殖を抑える様な競合的な相互関係だけでなく、時には他の菌の定着を助ける共生的な相互関係を築く事もあります。
■細菌同士の細胞~細胞シグナル
人体に於ける微生物の細胞‐細胞シグナルについては、最近まで殆ど明らかにはされてはいませんでした。しかし、2010年には、皮膚表面に最も定着する表皮ブドウ球菌が、セリンプロテアーゼであるEspを産生する事によって、病原性の高い黄色ブドウ球菌のバイオフィルム形成を阻害し、その上皮への定着を阻害する事が明らかになりました。2016年には、Staphylococcus lugdunensisが産生する抗菌ペプチドのlugduninが、黄色ブドウ球菌の増殖を抑えるだけでなく、何故か…長期投与にしても黄色ブドウ球菌はlugduninに対して耐性を獲得しない事が分かりました。これは、薬剤耐性の問題に悩まされ続けてきた黄色ブドウ球菌に対する有力な治療メカニズム!として大注目を浴びたので、ご存じの方も多いかも。2018年には、プロバイオティクスとして注目のBacillus属が産生するリポペプチドのfengycinsが、鼻腔及び腸管の黄色ブドウ球菌の定着を阻害する事が明らかになりました。fengycinsは、黄色ブドウ球菌の密度によって発動されるクオラムセンシングシステムを負に制御すると言う、裏技的クオラムクエンチングによって定着を防いでいるんだそうです。つまり、様々に異なる細胞-細胞シグナルを駆使して、病原性の高い日和見菌である黄色ブドウ球菌の定着を、他の細菌によって競合的に排除/阻害しているんです。
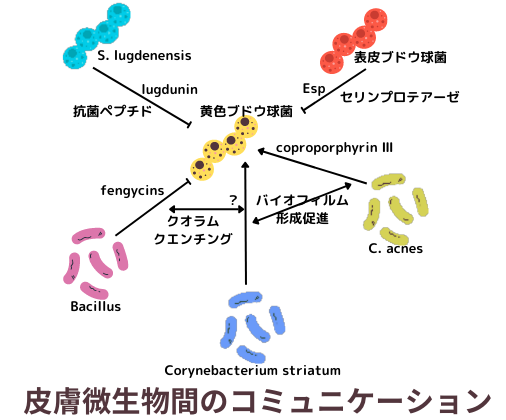 その一方で、黄色ブドウ球菌に肩入れして、その定着や増殖を促進する働きを担っている細胞-細胞シグナルもあります。ニキビの起因菌として知られるCutibacterium acnesが産生するcoproporphyrin Ⅲは、黄色ブドウ球菌を呼び集めて、バイオフィルムの形成のお手伝いをします。皮膚常在菌の一種であるCarynebacterium striatumは、黄色ブドウ球菌のクオラムセンシングによって発現する毒素の産生を抑制し、バイオフィルムの形成を促します。所謂病原菌から常在菌に近い様な振る舞いをする様に、遺伝子発現を変える作用も有しているんだそうです。これもクオラムセンシングシステムを負に抑制する、クオラムクエンチングの機序により惹起されると考えられています。
その一方で、黄色ブドウ球菌に肩入れして、その定着や増殖を促進する働きを担っている細胞-細胞シグナルもあります。ニキビの起因菌として知られるCutibacterium acnesが産生するcoproporphyrin Ⅲは、黄色ブドウ球菌を呼び集めて、バイオフィルムの形成のお手伝いをします。皮膚常在菌の一種であるCarynebacterium striatumは、黄色ブドウ球菌のクオラムセンシングによって発現する毒素の産生を抑制し、バイオフィルムの形成を促します。所謂病原菌から常在菌に近い様な振る舞いをする様に、遺伝子発現を変える作用も有しているんだそうです。これもクオラムセンシングシステムを負に抑制する、クオラムクエンチングの機序により惹起されると考えられています。
この様に、皮膚常在菌は、様々な細胞-細胞シグナルを介して、周囲と競合又は矯正する事で、皮膚表面の微生物叢を形成しているんです。まるで、HISAKOが毎朝散歩している美瑛川の堤防で繰り広げられている、熾烈な植物のホルモン戦争みたいです。
■周囲の細菌の数を検知して作動する、クオラムセンシング/クエンチングシステム
黄色ブドウ球菌が、周囲の細菌の数を感知して発動するクオラムセンシング/クオラムクエンチングシステムは、細胞-細胞シグナルの中でも特に重要と考えられており、細胞間のコミュニケーションの中核を担うものです。
クオセラムセンシングとは、フェロモン様の物質(クオルモン/別名・オートインデューサー)のやり取りによって、細菌が自分と同種の細胞が周辺にどれくらいの菌数、密度で存在しているかの情報を感知し、その情報に基づいて特定の物質の産生を行う機構の事です。オートインデューサーは、細胞内で転写制御因子に作用して、特定の蛋白質の合成を促進する働きを持っていますが、自分自身の細胞内で働くだけでなく、菌体外に分泌され、それが他の細胞内に取り込まれる事によって、その細胞にも作用します。
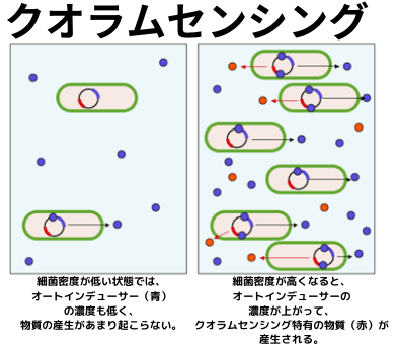 左図はWikipediaから引用した図ですが、少数の菌だけが生息している環境では、細胞内で合成されたオートインデューサーは細胞外に拡散し、結果的に細胞内の濃度は低くなります。その為、この様な環境下では、オートインデューサーによる転写促進はあまり強く働きません。しかし、多数の菌が生息している環境下では、これらの菌が環境中にオートインデューサーを分泌するので、濃度が上がり、細胞内の濃度も上昇します。その結果、オートインデューサーによってコントロールされている転写が促進され、その濃度が一定以上になった時に特定の物質産生が起きるという仕組みです。
左図はWikipediaから引用した図ですが、少数の菌だけが生息している環境では、細胞内で合成されたオートインデューサーは細胞外に拡散し、結果的に細胞内の濃度は低くなります。その為、この様な環境下では、オートインデューサーによる転写促進はあまり強く働きません。しかし、多数の菌が生息している環境下では、これらの菌が環境中にオートインデューサーを分泌するので、濃度が上がり、細胞内の濃度も上昇します。その結果、オートインデューサーによってコントロールされている転写が促進され、その濃度が一定以上になった時に特定の物質産生が起きるという仕組みです。
つまり、クオラムセンシングの機構によって、細菌はある程度以上の菌数(密度)に増殖するまで、特定の物質産生を抑制して、頭を垂れておとなしく生きています。しかし、十分な菌数が確保されると、特定の物質産生を行い、一気に攻めに転じます。一個一個の細菌は弱いので、菌数が少ない段階では敢て目立った行動を起こさずに地味に増殖を続け、それが多数に増えて安定した増殖が見込める状態になったら、クオラムセンシングを行って、機を逃さずに一気に繁殖するという戦略なんです。
緑膿菌やセラチア等の病原細菌が、日和見感染を起こしやすい理由の一つと考えられており、最近は、クオラムセンシングを阻害する物質によって、これらの感染症の予防や治療に役立てようとする研究が進められています。
アトピー性皮膚炎と黄色ブドウ球菌のクオラムセンシングシステム
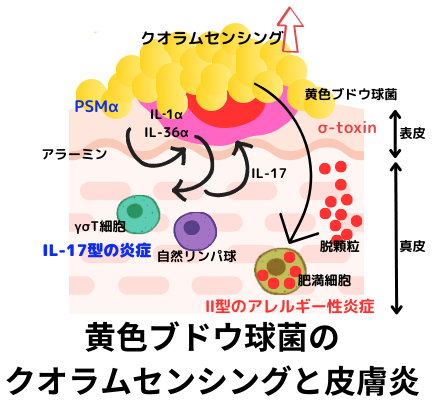 アトピー性皮膚炎の患者さんの皮膚は、健常な人の皮膚に比べ、黄色ブドウ球菌にモテモテで、大昔から取り憑かれ易い事は良く知られていました。
アトピー性皮膚炎の患者さんの皮膚は、健常な人の皮膚に比べ、黄色ブドウ球菌にモテモテで、大昔から取り憑かれ易い事は良く知られていました。
そのモテる理由を図説したのが、右です。皮膚の表面で黄色ブドウ球菌のクオラムセンシングシステムが発動すると、黄色ブドウ球菌がα‐トキシンを産生します。これは、皮膚の肥満細胞の脱顆粒を起こし、IL-4やIL-13等のサイトカインを放出させる事により、アレルギー性の皮膚炎を惹起させます。同時に、黄色ブドウ球菌が産生する毒素であるPSMαが、皮膚の最外層である表皮を構成するケラチノサイトにダメージを喰らわせ、IL-1αやIL-36等のアラーミンと呼ばれるサイトカインの放出を促します。これがIL-17依存性の皮膚炎を惹起します。これらの諸悪の根源であるα‐トキシンもPSMαも、どちらも、クオラムセンシングシステムに於けるAgr依存性に発現する事が分かっています。
真菌マイクロバイオーム
細菌が、ブドウ球菌属とキューティバクテリウム属、コリネバクテリウム属の三大勢力が、色んな体の部位によってその占有比率を争っているのと異なり、皮膚の真菌マイクロバイオームの中で最も勢力がある菌種は、体の部位に係らず(正しくは、足底部以外はなんですが)マラセチアちゃんです。つまり、皮膚の細菌達が、その属に係らす遭遇せざる得ないのがマラセチアって寸法なんです。尤も、14歳以下のガキんこの皮膚は、大人と比べて、より多くの種類の真菌が棲息しています。成長に伴う皮脂腺の増加や皮脂成分の変化に伴い、その多様性が失われ、大人では、マラセチアほぼ一択になっちゃうようですが。
マラセチアは、健康な人の皮膚にいる常在菌って奴ですが、私達宿主の状態によっては、脂漏性皮膚炎(美容通信2004年9月号)、癜風(美容通信2007年8月号)、マラセチア毛包炎、アトピー性皮膚炎(美容通信2007年4月号)の原因或いは増悪因子になります。脂漏性皮膚炎では、マラセチアが産生するリパーゼが皮脂を分解し、その分解産物である脂肪酸(特にオレイン酸)が炎症を惹起します。その一方で、マラセチアが分泌するアスパラギン酸プロテアーゼは、黄色ブドウ球菌のバイオフィルム形成を阻害します。この様に、マラセチアは、宿主である私達、若しくはマイクロバイオーム環境によって、病原性を示したり、健康維持にも働く…両刃の剣と言うよりはとっても人間らしい感性の持ち主!(笑)なんです。
真菌マラセチアMalasseziaの特徴
■菌学的特徴
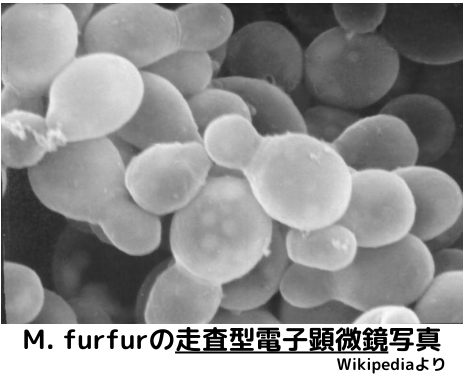
マラセチアってカビは、私達人間だけでなく、哺乳類の皮膚に常在し、所謂環境中には存在出来ない酵母様真菌です。大道芸人が作る風船みたいな形状で、大きさは約2~8×2~12μm。現在判明しているのは18菌種ですが、うち10菌種は人間様限定で、残り8種類は人間以外の、犬や猫、馬等の哺乳類に存在し、宿主特異性があります。
マラセチア自身は細胞内で脂肪酸を合成出来ないので、皮膚の上の皮脂を栄養源とするのですが、そのままでは利用出来ないので、自身が産生するリパーゼで、脂肪中のトリグリセリドのエステル結合を加水分解して、遊離脂肪酸を生成します。この分解産物はマラセチアだけのご飯になる訳ではなく、他の皮膚微生物のご飯にもなります。それどころか、オレイン酸等の一部の不飽和脂肪酸は、皮膚に炎症を引き起こす事があります。
真菌の一般的なゲノムサイズが約10~30Mbp以上(遺伝子は10000程度)なのに対し、マラセチアは7~8Mbpしかありません。保有遺伝子も約4000しかなく、他の真菌に比して生物学的な機能も限定的です。しかしながら、単に数が少ないだけの空っぽ野郎かと申しますと、これが、全く侮れない軽量進化系なんです。例えば、炭水化物代謝に関与する加水分解酵素をコードする遺伝子が大幅に喪失しているんですが、ちゃっかりリパーゼ遺伝子だけは10~15種と増量して、皮脂中に存在するあらゆる基質を加水分解出来る様に進化しているんです。
■真菌マイクロバイオームとしての特徴
マラセチアは皮脂を栄養源として増殖するので、皮膚の上の菌量は皮脂量で決まります。その為、皮脂腺が発達する思春期頃に、男女共にマラセチア定着量はぐ~んと増えますが、その後は年を取るにつれ減少します。皮膚のマイクロバイオームは、マラセチア関連皮膚疾患の患者さんも、罹患していない健常人も、M. restrictaとM. globosaの2菌種でほぼ構成されていますが、その構成比率は疾患ごとに特徴があります。脂漏性皮膚炎では、M. restrictaが優位なのに対し、癜風ではM. globosa優位です。アトピー性皮膚炎と尋常性乾癬(美容通信2008年4月号)(美容通信2019年9月号)では、M. restrictaとM. globosaの占有比率が約3:2なんです。
脂漏性皮膚炎への真菌の関与
■真菌マイクロバイオーム
脂漏性皮膚炎は、フケの塊がこびり付く皮膚の病気で、頭皮や髪の生え際、顔面等、皮脂量の多い部位(脂漏部)に好発します。その発症には、遺伝的、環境的或いは心理的要因も関与する他因子疾患ですが、マラセチアの関与が最も大きいと考えられています。しかしながら、細菌のマイクロバイオームについては、Cutibacterium属菌、Staphylococcus属菌、Sterptococcus属菌の3者が、病変部で有意に多いとされていますが、これらの細菌がマラセチアの定着にどの様に関与しているのかは、未だ解明されていません。
■病原因子としてのマラセチアリパーゼと皮脂代謝物
マラセチアは自身が産生するリパーゼで、皮脂を遊離脂肪酸に加水分解する事で栄養を確保します。それ故、餌の多い所にはマラセチア人口も多くなり、脂漏部には脂肪酸が溢れかえるなんて事態も発生します。この脂肪酸のうち、不飽和脂肪酸は、皮膚角化細胞の炎症性サイトカイン産生し、炎症を引き起こす元凶です。つまり、常在菌であるマラセチアが悪い訳ではないので、抗真菌薬で無用の殺生をするのではなく、病原因子であるリパーゼ活性を阻害する方が理には叶っているのではないのか。そんな新しい視点からの治療薬の探索が始まっています。
また、メタゲノム解析により、フケ頭の患者さんの頭に棲息しているM. restrictaのN-グリカン生合成経路の発現が亢進していたんだそうです。真菌の糖蛋白質は、宿主組織への接着に関与しているアロンαみたいなもんですから、この経路の発現亢進は、M. restrictaの環境に対する超進化!とも言えます。
■アリール炭化水素受容体と炎症
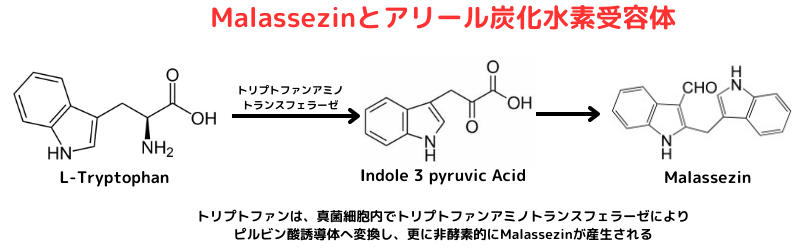
アリール炭化水素受容体は転写因子で、リガンドとの結合により種々の遺伝子の転写が活性化されます。
近年、このアリール炭化水素受容体が、慢性疾患にも係わっている事が知られて来ました。アトピー性皮膚炎や尋常性乾癬では、病変部のアリール炭化水素受容体が活性化しており、皮膚の炎症を起こしている可能性が指摘されています。実際、脂漏性皮膚炎の患者さんから分離されたM. furfurからMalassezinが単離されています。
マラセチアと細菌の相互作用
黄色ブドウ球菌は、皮膚に常在するブドウ球菌の中では毒性が高く、感染力は強い部類に属します。皮膚の上で、バイオフィルムを形成しながら増殖します。
バイオフィルムは、人間社会で強いて類似のコロニーを挙げるとしたら、ヒッピー達の理想卿・テイラーキャンプかな。それともノアの箱舟? 核シェルター? バイオフィルム内では、嫌気性菌から好気性菌、従属栄養から独立栄養のものまで様々な種類の微生物が存在し、相互に影響を及ぼし合い、栄養源を融通し合い、抗生物質や免疫に対する抵抗性を高めるなど、共同体として小宇宙(ミクロコスモス)を形成しています(←単一種のみで形成されるコロニーは、自然界には稀!)。形成後のバイオフィルムも、常に脱離や溶菌が起こり、ある程度大きくなると、コロニーが崩壊し、細菌が放出され、決して安定したものではないのも、正にテイラーキャンプ的ですよね。
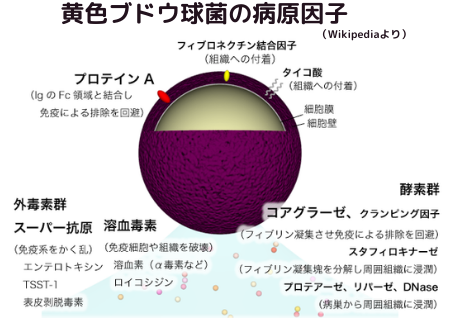 黄色ブドウ球菌の病原因子としては、①細胞に局在する病原因子(プロテインA・フィブロネクチン結合因子・タイコ酸 )、②細胞外に放出される毒素である外毒素(エンテロトキシン群・ TSST-1(毒素性ショック症候群毒素-1)・表皮剥脱毒素・溶血素(ヘモリジン)・ロイコシジン )、③病原性に関わる酵素群(コアグラーゼ、クランピング因子 ・スタフィロキナーゼ ・プロテアーゼ、DNase、リパーゼ)があります。プロテインAは細胞壁に存在する蛋白質で、黄色ブドウ球菌の主要な病原因子です。バイオフィルムの形成に必須な成分です。ところが、M. globosaには、15のアスパラギン酸プロテアーゼ(aspartic protease:Sap)がありますが、そのうちのMgSAP1は、黄色ブドウ球菌の生存率には影響を与えずに、プロテインAの分解を介して、バイオフィルムの形成を抑制します。昔は、プロテインAは、黄色ブドウ球菌を筆頭とするならず者帝国の陰の立役者と考えられていましたが、皮膚の上で最大勢力を誇る真菌であるマラセチアを常に隣人とせざる得ない以上、致命的なアキレス腱になる可能性があります。つまり、マラセチアは、宿主に有益な作用を齎す真菌の側面を有しています。
黄色ブドウ球菌の病原因子としては、①細胞に局在する病原因子(プロテインA・フィブロネクチン結合因子・タイコ酸 )、②細胞外に放出される毒素である外毒素(エンテロトキシン群・ TSST-1(毒素性ショック症候群毒素-1)・表皮剥脱毒素・溶血素(ヘモリジン)・ロイコシジン )、③病原性に関わる酵素群(コアグラーゼ、クランピング因子 ・スタフィロキナーゼ ・プロテアーゼ、DNase、リパーゼ)があります。プロテインAは細胞壁に存在する蛋白質で、黄色ブドウ球菌の主要な病原因子です。バイオフィルムの形成に必須な成分です。ところが、M. globosaには、15のアスパラギン酸プロテアーゼ(aspartic protease:Sap)がありますが、そのうちのMgSAP1は、黄色ブドウ球菌の生存率には影響を与えずに、プロテインAの分解を介して、バイオフィルムの形成を抑制します。昔は、プロテインAは、黄色ブドウ球菌を筆頭とするならず者帝国の陰の立役者と考えられていましたが、皮膚の上で最大勢力を誇る真菌であるマラセチアを常に隣人とせざる得ない以上、致命的なアキレス腱になる可能性があります。つまり、マラセチアは、宿主に有益な作用を齎す真菌の側面を有しています。
皮膚常在菌を操って、炎症性皮膚疾患を治療する時代が来るかも
アトピー性皮膚炎の皮膚では、アトピー性皮膚炎の重要な病態増悪因子である黄色ブドウ球菌が高頻度に定着している事が知られています。しかしながら、アトピー性皮膚炎の治療に抗菌剤を使用しても、その効果は一般的に乏しく、黄色ブドウ球菌を標的とした効果的な治療は未だ確立されていません。
未だ、実験のレベルで、確立された治療方法ではありませんが、最近は、黄色ブドウ球菌に対して、殺菌作用及び毒素抑制作用を有する人間の皮膚常在菌株を細菌移植する方法等も試みられています。糞便微生物移植法(美容通信2024年1月号)の皮膚バージョンですね。
皮膚常在菌は、宿主防衛機能を有した「THE 地球防衛軍」!
■抗菌活性
哺乳類の皮膚には、元々、病原性細菌の定着や日和見感染に対する宿主防衛機構が備わっています。地球防衛軍(EDF)の一翼を担う兵士には、Cathelicidinやβ‐defensin等の抗菌ペプチドがあります。これらは、細菌、ウィルス、真菌等の幅広い微生物に対し、殺菌活性を有する生体防衛物質です。つまり、地球防衛軍にも即応予備自衛官制度みたいなものが皮膚にも存在し、私達の皮膚の上では、抗菌ペプチドは、感染、バリア破壊、炎症等に伴い、迅速に発動(発現誘導)され、病原性微生物を排除してくれますが、通常の健康な皮膚の状態では、これらの抗菌ペプチドの発現量や、その他の免疫システムの活性は低く保たれています。兵隊が大勢いる戦時ではなく、平時にも平和が保たれる≒感染が起こらないですんでいるのは、皮膚に定着している常在細菌が様々な抗菌物質を産生し、皮膚表面に幾重もの化学的なバリアを構築しているからです。江戸時代の五人組・十人組の様な、村落内の相互扶助的な行政下部組織としての役割を、皮膚の常在細菌叢が担っているんですね。
■クオセラムセンシング抑制機能
私達人間の健常皮膚の常在菌叢に有意に定着しているCoNS(coagulase-negative staphylococcus)の中には前述の様に、抗菌物質を産生する菌株が存在します。更には、S. aureusのクオセラムセンシングを阻害するAIP(autoinducing peptide)と呼ばれる、低分子環状ペプチドを産生する菌株も存在する事が分かって来ました。
S. aureusに対する抑制的な作用は、CoNS種だったら誰もが有している作用って訳ではなく、限られた菌株のみの特権なんだそうです。しかしながら、コンフォート研究によると、抗菌活性やクオセラムセンシング抑制機能を有するCoNS株は、健常な皮膚に優位に定着しており、皮膚の恒常性や防衛機能の維持に大きく寄与していると考えられています。
アトピー性皮膚炎では、皮膚防衛機能が低下している
常在菌叢の多様性が減少した、若しくはそのバランスが崩壊した状態を、ディスバイオーシスと言います。この様な状態は、宿主の健康を損なう大いなる外的要因となります。
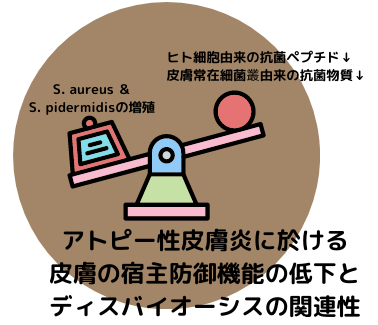 例えば、アトピー性皮膚炎の皮膚では、IL-4やIL-13等のTh2サイトカインの所為で、感染を排除するに十分に足るだけの量の、cathelicidinやβ-dfensin等の抗菌ペプチドの産生が行われないので、S. aureusの定着や、表皮ブドウ球菌の一種であるStaphylococcus epidermidisの異常増殖が高頻度で起こっています。軟弱な保安官を尻目に、ならず者達が乱暴狼藉を働くマカロニ・ウェスタンの世界が、アトピー性皮膚炎の皮膚の上で展開されているようなものですね(笑)。荒野の用心棒ならぬ、デュピルマブ製剤「デュピクセント」(美容通信2019年7月号)で、IL-4及びIL-13を拮抗すると、S. aureusの定着数が低下し、常在細菌叢の多様性は回復します。Th2型炎症に伴う自然免疫機能低下が、ディスバイオーシスと関連しているんだなぁと、つくづく実感させられるお薬です。
例えば、アトピー性皮膚炎の皮膚では、IL-4やIL-13等のTh2サイトカインの所為で、感染を排除するに十分に足るだけの量の、cathelicidinやβ-dfensin等の抗菌ペプチドの産生が行われないので、S. aureusの定着や、表皮ブドウ球菌の一種であるStaphylococcus epidermidisの異常増殖が高頻度で起こっています。軟弱な保安官を尻目に、ならず者達が乱暴狼藉を働くマカロニ・ウェスタンの世界が、アトピー性皮膚炎の皮膚の上で展開されているようなものですね(笑)。荒野の用心棒ならぬ、デュピルマブ製剤「デュピクセント」(美容通信2019年7月号)で、IL-4及びIL-13を拮抗すると、S. aureusの定着数が低下し、常在細菌叢の多様性は回復します。Th2型炎症に伴う自然免疫機能低下が、ディスバイオーシスと関連しているんだなぁと、つくづく実感させられるお薬です。
更に、憂慮すべき状況としては、抗菌物質を産生する皮膚常在菌も減少している事です。皮膚に常在するCoNS(coagulase-negative staphylococcus)群のS. aureusの排除能を調べると、健常皮膚から単離された多くのCoNS株は抗菌活性を示しましたが、アトピー性皮膚炎の皮膚では抗菌活性を示すCoNS株は非常に稀! 稀有な存在!なんだそうです。また、S. aureusは、抗菌活性を有するCoNS株が大多数を占めている様な皮膚環境では、付け入る隙間もないので、定着だって出来ません。
つまり、この様にアトピー性皮膚炎に伴うディスバイオーシスは、宿主の自然免疫反応及び皮膚常在細菌叢を介した宿主防御機能の低下に起因しているんです。
アトピー性皮膚炎の治療としての皮膚常在菌移植
実験のレベルで、未だ確立された治療方法ではありませんが、黄色ブドウ球菌に対して、殺菌作用及び毒素抑制作用を有する人間の皮膚常在菌株を細菌移植する方法等も試み始められています。先月号(美容通信2024年1月号)でも触れた、糞便微生物移植法の皮膚バージョンですが、発売されたら、HISAKOのクリニックでも是非取り扱いしたいなと思っています。
試験では、抗菌活性を有するCoNS株の生菌含有のクリームを1週間塗布し、その後塗布終了後96時間後まで経過観察を行ったそうです。生菌の出所は、自分のもの(自家移植)と他人のもの(他家移植)の両方で行いましたが、そのどちらに於いても、生菌を移植した部位では、投与4日目と言う驚異的に早い段階で、基剤のクリームだけを塗布した群と比して、S. aureusの生存率は1%以下に減少し、その抗菌活性は治療終了後96時間まで持続していたんだそうです。アトピー性皮膚炎の評価スケールであるEASIスコアの改善率も、S. aureusの減少数と、統計学的に有意な正の相関関係があったそうです。つまり、とっとと皮膚炎が良くなってしまったんです。
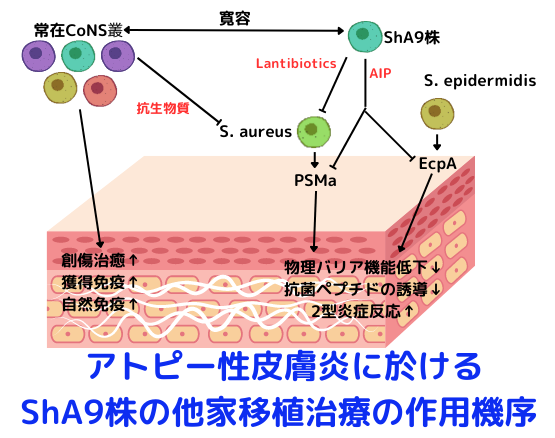 また、ShA9株は、lantibioticを産生して、黄色ブドウ球菌を直接排除します。それだけではなく、AIPにより、S. aureusやS. epidermidisのクオラムセンシング制御下にある毒素や蛋白質分解酵素の発現を抑制し、アトピー性皮膚炎を改善します。更に、常在細菌叢の多様性を正常化する事でも、皮膚の恒常性の維持に貢献します。
また、ShA9株は、lantibioticを産生して、黄色ブドウ球菌を直接排除します。それだけではなく、AIPにより、S. aureusやS. epidermidisのクオラムセンシング制御下にある毒素や蛋白質分解酵素の発現を抑制し、アトピー性皮膚炎を改善します。更に、常在細菌叢の多様性を正常化する事でも、皮膚の恒常性の維持に貢献します。関連ページ
関連するHISAKOの美容通信をピックアップしました。
来月号の予告
単なる掃除屋と侮るなかれ! あらゆる疾患を制御する機能性多様性が、今、漸く、明らかになりつつあります。
<シン・マクロファージ>